I cent’anni della Meccanica Quantistica
La relazione con i concetti classici della chimica e didattica
Giovanni Villani
Coordinatore del Gruppo Tematico Epistemologia e Storia della Chimica
della Società Chimica Italiana
e-mail: giovanni.villani@cnr.it
Indice
2. Dalle proprietà atomiche a quelle molecolari
3. La trattazione quantistica delle reazioni chimiche: storia e prospettive
4. Le sfide nell’insegnamento della meccanica quantistica nella scuola secondaria di secondo grado
Abstract. The United Nations General Assembly has designated 2025 as the “International Year of Quantum Science and Technology”. Quantum science, in fact, provides the foundation for basic research and the interpretation of the atomic/molecular world, and its beginning can be dated back to the works of Heisenberg and Pauli in 1925. The study of the molecular world, however, did not begin that year. Nineteenth-century chemists, in fact, developed useful concepts in this world and connected them to the macroscopic properties of chemical substances. In this educational paper, we intend to discuss the conceptual aspects and “open issues” of the relationship between quantum mechanics and the historical concepts of chemistry. Although this physical theory represented a revolutionary change in the study of the atomic/molecular world, it still struggles to gain traction in the educational and general/cultural contexts, both for “objective” reasons and due to the current lack of attention to the analysis of the conceptual/philosophical problems of this theory and their educational treatment.
Keywords: meccanica quantistica; rapporto con la chimica classica; didattica
È passato un secolo da quando la meccanica quantistica ha dispiegato le sue potenzialità nell’analizzare il mondo sub-microscopico della materia. Tale mondo è fondamentale per l’interpretazione chimica dell’universo che ci circonda. Alla nascita della meccanica quantistica ha concorso in maniera evidente lo studio dell’atomo e della sua struttura. Ben noti sono i modelli atomici di inizio Novecento che, a partire da Bohr, hanno introdotto la quantizzazione dell’energia nell’atomo. Ben presto, però, l’analisi dell’atomo come sistema di molti costituenti è stata affiancata dalla riflessione su cosa tenesse insieme un gruppo di atomi, formando una molecola.
La molecola, infatti, più ancora che l’atomo, era stato un problema difficilmente razionalizzabile nella scienza atomistica del XIX secolo. Un atomo nel senso letterale del termine, cioè un pezzo di materia dotato di massa, con o senza una sua propria forma specifica, ma “chiuso in sé stesso” faceva fatica a spiegare l’interazione con gli altri atomi e, ancora di più, l’interazione selettiva collegata alle affinità chimiche delle sostanze.
I fisici, fin dal XVII secolo, avevano relazionato l’interazione tra le particelle, e quindi anche quelle microscopiche tra gli atomi, a due concetti: quello di urto e quello di forza. Vi era, quindi, da un lato, una visione dell’interazione come istantanea e a contatto (urto) e, dall’altro lato, come permanente e dipendente dalla distanza, assimilata alla forza gravitazionale e/o elettrica. In quest’ultima visione, gli stessi atomi potevano essere “dematerializzati” a punti di forza dotati di massa [1]. I chimici, invece, da Dalton in poi, avevano concettualizzato gli atomi come particelle di materia, differenziate per massa (il cosiddetto “peso atomico”). La variazione del peso atomico degli elementi (e relativi atomi che li costituivano), tuttavia, appariva difficilmente spiegabile, non trovando delle facili regolarità: il peso atomico, infatti, non variava né linearmente né in forme più complesse ma razionalizzabili, come quella cubica che avrebbe relazionato il peso atomico al volume della particella. Vi era, poi, il problema della periodicità tra le proprietà chimiche degli elementi evidenziate dalla Tavola Periodica di Mendeleev. Questi problemi erano impossibili da capire senza penetrare all’interno dell’atomo.
Dopo la scoperta dei componenti atomici, prima l’elettrone, poi il nucleo e, infine, la sua differenziazione in protoni e neutroni, il problema della struttura atomica non poteva più essere eluso. La soluzione trovata nel XX secolo ha fuso insieme l’immaterialità (punti di forza) dei fisici e la materialità (particella di materia) dei chimici in un mondo atomico duale, un’onda/particella sia per i costituenti atomici sia per l’intero atomo. Il concetto di molecola, invece, è stato definito come un gruppo di atomi con posizioni definite stabile dal punto di vista energetico.
Dopo cent’anni di meccanica quantistica, restano ancora da capire se e come alcune caratteristiche teoriche/generali di tale teoria fisica si possono rapportare ai concetti elaborati dalla tradizione chimica. Questo argomento è troppo vasto per essere analizzato in dettaglio in questo lavoro e, quindi, qui analizzeremo solamente come la visione quantistica fisica e chimica sviluppano il rapporto tra le caratteristiche degli enti atomici e quelli molecolari. Chiuderemo il lavoro con delle considerazioni didattiche su come e quando introdurre le problematiche quantistiche a scuola e all’università.
2. Dalle proprietà atomiche a quelle molecolari
In questo paragrafo cercheremo di dare una risposta su come la meccanica quantistica e la chimica classica connettono le proprietà atomiche a quelle molecolari e, quindi, dall’ente atomico a quello molecolare.
Per dare una risposta alla domanda sulla differente connessione tra le proprietà atomiche e quelle molecolari in questi due ambiti, dobbiamo ricordare il diverso significato che hanno le parti di un sistema per questi due ambiti scientifici. La meccanica quantistica è una teoria olistica, nel senso che vuole calcolare gli stati stazionari del sistema globale studiato e tali stati sono distribuiti su tutto il sistema e non identificano relazioni particolari tra i costituenti. Questo non significa, ovviamente, che sono stati globali distribuiti uniformemente su tutti i costituenti, ma i costituenti e i loro stati sono parti del tutto all’interno del sistema e non hanno più, quindi, una loro realtà indipendente. Anche quando tale teoria utilizza gli stati dei componenti per ottenere questi stati globali, come nella impostazione LCAO-MO degli stati elettroni molecolari, dove gli stati stazionari globali della molecola (molecular orbital, MO) sono una combinazione lineare degli orbitali dei componenti atomici (linear combination of atomic orbitals, LCAO), gli stati dei costituenti sono una delle possibili basi (in senso matematico) per la costruzione degli stati stazionari del sistema molecolare globale. Gli stati atomici (e, con essi, i relativi sistemi atomici) perdono all’interno della molecola qualsiasi significato “reale” e la loro combinazione (i coefficienti della combinazione lineare nell’approccio LCAO) servono solo come una possibile determinazione dello stato globale. Una qualsiasi altra base matematica, per esempio una distribuita equamente nello spazio molecolare, potrebbe svolgere lo stesso scopo. Ovviamente, dovendo descrivere sia gli elettroni interni, che restano vicino ai nuclei atomici anche nelle molecole, sia quelli di legami, distribuiti su tutto lo spazio molecolare, tale base necessiterebbe di più funzioni, alcune che restano essenzialmente localizzate intorno ai nuclei ed altre diffuse su tutto il sistema. La dimensione della base, cioè il numero di funzioni necessarie, in questo caso, sarebbe maggiore.
La chimica, invece, e quindi anche la chimica quantistica, ritiene che sia utile “connettere” gli stati molecolari e le relative proprietà agli stati atomi e alle proprietà degli atomi.1 Questo non significa che il chimico quantistico ritenga che gli stati atomici continuino a esistere nella molecola. Avendo, tuttavia, come fine non solo quello di calcolare le proprietà molecolari, ma anche quello di “proiettarle” sugli atomi costituenti per consentire di comparare e raggruppare le molecole, ritiene che i costituenti (sia gli stati sia gli enti) continuino a essere essenziali.
L’importanza degli atomi nella molecola è evidenziata dalla formula chimica che ci dice che la molecola dell’acqua è formata da 2 atomi d’idrogeno e uno di ossigeno, H2O. Va, tuttavia, precisato che per il chimico, sebbene usi gli stessi simboli (H e O), questo non significa che l’idrogeno e l’ossigeno nell’acqua siano uguali a quelli degli atomi isolati e neppure a quelli degli stessi atomi presenti in altre molecole: essi sono degli atomi in situ, cioè nelle condizioni specifiche della molecola [2]. Talvolta, questo viene evidenziato sovrascrivendo agli atomi delle cariche parziali (δ+ e δ-), ma anche quando non ci sono cariche parziali, come nella situazione degli elementi poliatomici, per esempio l’atomo d’idrogeno in H2 e quello di ossigeno in O2, gli atomi costituenti una molecola sono diversi dagli atomi isolati.
Inoltre, possiamo dire che per la meccanica quantistica il concetto di molecola è meno rilevante che per la chimica. Consideriamo l’esempio di due isomeri e analizziamo la particella elementare di C2H6O. Per il chimico esistono due molecole, C2H5OH e CH3OCH3, ricollegabili alla formula bruta C2H6O: esse sono le particelle elementari di due sostanze molto differenti. La prima è l’alcol etilico, sostanza liquida a temperatura ambiente e che viene utilizzato, per esempio, per preparare le bevande alcoliche; la seconda è l’etere dimetilico, una sostanza gassosa a temperatura ambiente e tossico per l’uomo ed è “parente” del famoso etere (etere dietilico) che in passato veniva usato come anestetico (Figura 1). Tali molecole, quindi, corrispondono a due sostanze macroscopiche con proprietà molto differenti.

Figura 1. 30 marzo 1842: primo intervento chirurgico con l’uso dell’etere come anestetico
Nella descrizione quantistica di C2H6O si costruisce la superficie di energia potenziale multidimensionale di questo sistema e si nota che esistono due minimi molto marcati: uno relativo alla particella elementare con un atomo d’idrogeno vicino all’atomo d’ossigeno e un’altra senza questa particolarità. Notiamo che questo discorso può essere fatto solo nell’approssimazione di Born-Oppenheimer, quella che considera un approccio di meccanica classica per i nuclei atomici e ne fissa le posizioni. Tale approssimazione può essere evitata nella trattazione quantistica di qualche sistema molecolare semplice, ma, in questo caso, si accentuano i problemi con l’ottica chimica. Nella meccanica quantistica, infatti, i componenti atomici dello stesso tipo non possono essere differenziati. Non possiamo, per esempio, identificare differenti tipi di elettroni, neppure posizionandoli sugli atomi: quello sull’atomo 1, quello sull’atomo 2, eccetera, ma dobbiamo permutare tutti gli elettroni su tutti gli atomi per ottenere un solo tipo di elettrone. Se queste permutazioni venissero applicate anche agli atomi, nell’esempio della molecola dell’alcol etilico non potremmo più distinguere differenti tipi di atomi d’idrogeno [3]. Per il chimico, invece, è essenziale distinguere tra i due i tipi di atomi d’idrogeno presente nell’alcol etilico (C2H5OH): quelli legati agli atomi di carbonio da quello legato all’atomo di ossigeno. Non sarebbe, quindi, più possibile associare questa sostanza alla categoria degli alcoli per la presenza di un gruppo funzionale O–H [4].
L’esistenza all’interno della stessa molecola di più tipi di atomi dello stesso elemento, sebbene indicati con lo stesso simbolo, è essenziale per spiegare alcune proprietà delle sostanze chimiche e, in particolare, la loro reattività. Per esempio, la differenza di reattività tra gli eteri e gli alcoli, o quella tra gli eteri e i composti carbonilici nel caso di due tipi di atomi di ossigeno differenti all’interno della stessa molecola, è legata a specifici atomi nella molecola. Tutta la chimica organica, e buona parte della biochimica, utilizzano queste specificità.
Quindi, la sola prospettiva quantistica fisica risulta insufficiente in questi casi per importanti problematiche conoscitive della chimica perché essa deve rispondere a suoi interrogativi specifici, come quelli sulla reattività.
3. La trattazione quantistica delle reazioni chimiche: storia e prospettive
Dopo aver considerato come la fisica e la chimica quantistica trattano le proprietà delle molecole, andiamo a occuparci della proprietà di trasformazione delle molecole: le reazioni chimiche. Iniziamo con il guardare come la nascente meccanica quantistica fu collegata al problema storico dello studio delle reazioni chimiche. Fra il 1915 e il 1940 furono oggetto di un’intensa rielaborazione due gruppi di problemi riguardanti la trattazione teorica delle reazioni chimiche: il meccanismo delle reazioni, cioè l’identificazione di tutte le tappe dello svolgersi di una reazione chimica, e la natura dell’atto elementare della reazione [5, 6].
In questo contesto, vogliamo sottolineare un aspetto generale di filosofia della scienza poco noto, ma indicativo. Il concetto di meccanismo di reazione ha acquisito in questo inizio del XXI secolo un ruolo sempre più generale e importante nella spiegazione scientifica della realtà [7, 8]. All’articolo di Machamer, Darden e Craver intitolato Thinking about mechanisms è stata collegata la nascita di una nuova corrente filosofica, quella denominata New mechanism philosophy. Questa nuova corrente filosofica è nata da esempi di biologia e di neuroscienze (Machamer è un filosofo e storico della scienza, Darden una filosofa della biologia e Craven un filosofo delle neuroscienze), ponendo nessuna attenzione al concetto di meccanismo dei processi chimici utilizzato da un secolo dai chimici, come ha sottolineato il filosofo della chimica Robin Hendry nel suo lavoro sul meccanismo in chimica [9]. È, quindi, importante a nostro avviso che, chi si occupa di filosofia della chimica e del ruolo culturale che questa disciplina ha avuto (e ha) all’interno delle scienze naturali, rivendichi il ruolo che storicamente la chimica ha svolto nell’elaborazione del concetto di meccanismo di un processo.
Nella chimica teorica attuale, l’approccio principale allo studio delle reazioni chimiche è la teoria dello stato di transizione (TST), anche nota come “Teoria della velocità assoluta di reazione” o “Teoria del complesso attivato”, le cui radici risalgono all’inizio del Novecento.
La teoria statistica delle reazioni chimiche parte con il lavoro di Marcelin del 1915 [10]. È poi sviluppata principalmente da Eyring nel 1935 [11], per calcolare la “velocità assoluta di reazione” nelle reazioni bimolecolari, e da Evans e Polanyi come teoria dello “stato di transizione” [12, 13]. L’idea di base di questa teoria è che durante la reazione il sistema debba superare una regione critica (stato di transizione o complesso attivato) nello spazio delle configurazioni2 per passare dallo stato iniziale (regione dei reagenti) allo stato finale (regione dei prodotti). Assumendo la distribuzione di equilibrio termico negli stati iniziali dei reagenti e negli stati del complesso attivato, fu derivata, sulla base della meccanica statistica, la formula per la velocità di reazione in funzione delle probabilità di trovare il sistema nello stato iniziale e nello stato finale, della velocità media con la quale il sistema passa nella stretta regione attivata dello spazio delle configurazioni e della probabilità che il sistema, passato lo stato di transizione, raggiunga lo stato finale dei prodotti [14, 15]. In seguito, Pelzer e Wigner [16] introdussero l’uso delle superfici di energia potenziale in questa trattazione statistica delle reazioni chimiche, identificando lo stato di transizione con il punto di sella (minimo di energia in tutte le coordinate meno una nella quale abbiamo un massimo di energia) di una superficie potenziale (Figura 2).
Il percorso di minima energia che connette i reagenti, lo stato di transizione e i prodotti, identifica quello che viene chiamato “cammino di reazione” (indicato con la curva continua in rosso nella parte alta di figura 2). Furono Hirshfelder e Wigner [17] che per primi discussero la validità della teoria del complesso attivato dal punto di vista della meccanica quantistica. Essi mostrarono che la nozione di complesso attivato era compatibile con il principio di indeterminazione di Heisenberg solo quando la variazione dell’energia potenziale lungo il cammino di reazione nella regione del complesso attivato era “sufficientemente piatta”.
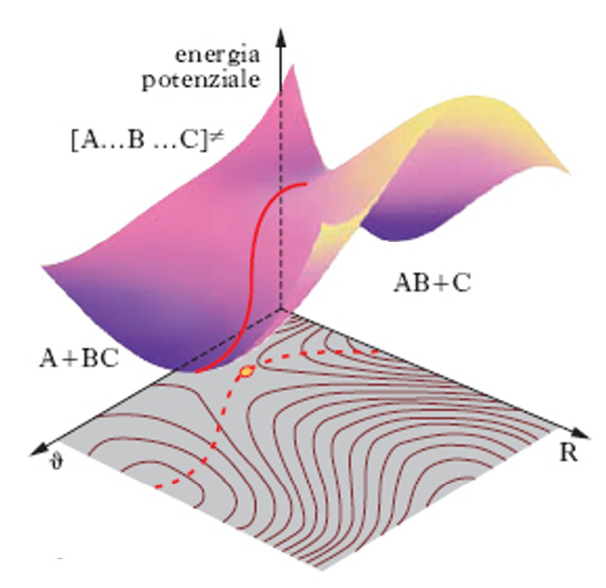
Figura 2. Generica curva di energia potenziale per la reazione A + BC → AB + C (in alto) e sua proiezione nel piano (in basso)
Questa condizione era necessaria sia per la definizione di “complesso attivato” sia per il movimento di traslazione lungo la coordinata di reazione. Solo se tale condizione fosse stata rispettata, infatti, il movimento lungo la coordinata di reazione poteva essere descritto dalla meccanica classica. Tale condizione, tuttavia, non era sufficiente da sola per la definizione del complesso attivato come una configurazione stabile. Era necessario, infatti, assumere che il tempo di vita del complesso attivato fosse sufficientemente da far sì che, mentre il sistema passava nella regione intermedia dello spazio delle configurazioni, avvenissero molte vibrazioni e rotazioni per il complesso attivato. In pratica, la teoria del complesso attivato era giustificata in presenza di un movimento lungo la coordinata di reazione così lento da far variare con continuità gli stati del complesso attivato. Ciò assicurava la possibilità di trattare in maniera quantomeccanica sia gli stati del complesso attivato sia la loro distribuzione di equilibrio termico.
Analizziamo adesso i concetti fondamentali su cui si basa la TST. Nella teoria cinetica delle collisioni si suppone che le molecole siano non interagenti tranne che in un infinitamente breve lasso di tempo in cui si urtano. Sono questi urti che permettono la distribuzione di Boltzmann tipica dell’equilibrio termico delle velocità molecolari e, quando casualmente le molecole superano, come energia scambiata, una soglia prefissata, innescano la reazione. Dietro questa teoria c’è una visione da meccanica classica delle molecole. Esse sono dei gruppi di palline che urtandosi si separano. Il problema è che questa visione semplicistica può andare bene solo per pochi tipi di reazione, in particolare per le reazioni unimolecolari. Sono, infatti, queste le reazioni in cui due molecole della stessa specie si urtano e una delle due acquista un’energia che la porta a dividersi in frammenti. In generale, una reazione chimica porta a una globale ristrutturazione delle molecole implicate nell’urto, così globale da dare vita ad altre molecole. Una teoria delle reazioni deve, quindi, spiegare i complessi meccanismi che permettono di sostituire atomi e formare selettivi legami, oltre che spiegare la rottura di alcuni legami. È per così dire la parte di “riorganizzazione” delle molecole più che la parte di rottura a mancare. A nostro avviso, tale teoria è ancora legata sostanzialmente al concetto di molecola come “insieme di sfere rigide”, cioè sistema in cui “struttura molecolare” coincide con “disposizione” degli atomi. Noi, invece, abbiamo già mostrato [5, 6] che, oltre alla variazione delle posizioni degli atomi, una reazione chimica può essere vista come “una disorganizzazione seguita da riorganizzazione”. Inoltre, tale teoria cerca di interpretare tutti i fenomeni sotto un aspetto puramente meccanicistico e non considera le specifiche interazioni chimiche. Questa problematica diventa sempre più evidente all’aumentare della dimensione molecolare e, quindi, per le macromolecole. I siti attivi ed allosterici delle proteine [18] ne sono un ottimo esempio.
Concludendo questo paragrafo, le trasformazioni chimiche sono una parte fondamentale dell’approccio chimico allo studio del mondo materiale. Per questa scienza, infatti, i milioni di enti che la caratterizzano, le molecole nel piano microscopico e le sostanze chimiche in quello macroscopico, sono il plurale qualitativo del mondo, ma sono anche la base con cui spiegare la sua trasformazione. La capacità di tenere insieme tanto gli aspetti statici, proprietà degli enti, quanto quelli dinamici, loro trasformazione, è il risultato storico di una scienza che ha sempre dato una notevole importanza all’aspetto di varietà e trasformabilità della materia.
4. Le sfide nell’insegnamento della meccanica quantistica nella scuola secondaria di secondo grado
Andiamo adesso ad analizzare gli aspetti didattici della meccanica quantistica, in particolare lo studio quantistico del mondo atomico/molecolare nelle scuole secondarie di secondo grado. Una problematica simile si riscontra anche nel suo insegnamento all’inizio dell’università.
La meccanica quantistica è spesso considerata troppo avanzata per tali studenti e sorgono diverse sfide nel cercare di insegnarla. Queste includono concetti astratti (come la dualità onda-particella, la configurazione elettronica e i numeri quantici) e la necessità di una solida preparazione matematica. Esiste, tuttavia, una crescente quantità di ricerche su come insegnare e apprendere la meccanica quantistica a livello di scuola secondaria di secondo grado, con un focus sul miglioramento della comprensione concettuale [19-23]; anche in Italia ci si è occupati di queste problematiche generali [24, 25], sull’uso di simulazioni computerizzate [26, 27] e sull’integrazione di applicazioni reali. A volte si può ricorrere a un “gioco” per superare le difficoltà concettuali [28].
Se questa è la situazione internazionale, possiamo notare un “ritardo” della scuola italiana nello studio di questo argomento. Sebbene questo sia uno dei problemi generali della impreparazione scientifica, c’è anche il problema opposto, cioè quello di accennare, senza poter chiarire, i concetti del mondo atomico/molecolare ad alunni della primaria. Io credo che sia ormai impossibile non utilizzare i termini di atomo e molecola con gli studenti di tutte le età, perché il “mondo esterno” alla scuola utilizza tali termini ormai a ogni livello di informazione, dalla pubblicità in avanti. In tutti i casi, questo non è “studiare gli atomi e le molecole” e ancora di più non è, e non può essere, studiare gli atomi e le molecole della scienza contemporanea.
La mia idea è che l’età migliore per iniziare uno studio sistematico del mondo submicroscopico sia il terzo anno delle scuole secondaria di secondo grado. Attualmente, non è questa la situazione del Liceo Scientifico tradizionale. Se si guarda ai testi scolastici di Chimica più diffusi, l’atomo e la molecola quantistica sono trattati nel volume del primo biennio. Le Indicazioni Nazionali riguardanti gli obiettivi specifici di apprendimento per il Liceo Scientifico, invece, recitano che al primo biennio si dovrebbero trattare le leggi fondamentali e il modello atomico di Dalton, lasciando al secondo biennio “lo studio della struttura atomica e dei modelli atomici, il sistema periodico, le proprietà periodiche e i legami chimici”.
Il passaggio dalla meccanica classica a quella quantistica è uno snodo culturale, oltre che tecnico. Esso andrebbe trattato e approfondito, quanto possibile, in maniera interdisciplinare. All’inizio del XX secolo, infatti, in quasi tutti gli ambiti culturali sono avvenute “rivoluzioni” che hanno scardinato l’immagine classica e semplice del mondo. Fare anche solo intuire allo studente che la complessità dell’odierna visione scientifica del mondo possa essere ricollegata alla complessità dell’arte contemporanea, per esempio, sarebbe un punto culturale importante.
L’approccio al mondo quantistico è ricco di implicazioni filosofiche ed epistemologiche che vanno esplicitate, nei limiti del possibile. Per esempio, se non è chiaro il concetto di modello scientifico è difficile far capire agli studenti perché si considerano “tanti” modelli atomici [29].
Il mondo atomico e molecolare va introdotto a scuola seguendo il percorso storico che ha portato alla sua nascita e al successivo consolidamento nel mondo quantistico. È vero che attualmente questi argomenti scolastici della scienza sono tra i pochi introdotti con riferimenti storici (il modello atomico di Thomson prima del modello atomico di Bohr, per esempio), ma spesso in tale approccio scolastico manca la problematicità storica, mancano le motivazioni culturali e non solo che hanno “costretto” gli scienziati a superare un modello di atomo per passare a un altro. Senza questi “collegamenti”, la trattazione storica di questi argomenti diviene un susseguirsi di modelli senza un filo logico.
Anche alcuni aspetti “tecnici” della proposta didattica della meccanica quantistica vanno, a mio avviso, rivisti come, per esempio, l’impostazione, seguita da molti libri di testo, di partire dalla doppia natura onda-particella della luce e della materia come primo argomento da trattare nell’introduzione alla quantistica. L’idea generale sottesa a tale scelta è che, dopo aver introdotto la doppia natura della luce e della materia, si possa passare “naturalmente” all’equazione di Schrödinger e poi agli orbitali. Quest’ordine di trattazione è, a mio avviso, sbagliato perché, oltre a essere falso storicamente, rischia di far mancare il graduale passaggio tra l’orbita dell’elettrone della meccanica classica, l’orbita quantizzata di Bohr e il concetto di orbitale (il cui stesso nome è collegato, non causalmente, all’orbita), togliendo a quest’ultimo concetto il suo ancoraggio storico. In pratica, bisogna procedere con la meccanica classica fino al modello atomico di Bohr (e di Sommerfeld, se si vuole accennare a tale modello) e, solo dopo aver introdotto la quantizzazione delle orbite, introdurre la doppia natura della luce e della materia.
Resta poi da capire quale materia scolastica dovrebbe occuparsi di questo studio, cioè dove inserire lo studio dell’approccio quantistico. Sicuramente la meccanica quantistica va studiata al liceo al quinto anno nell’ambito della fisica. Ad essa e alla meccanica relativistica è riservato un posto importante nelle Indicazioni ministeriali per il quinto anno del liceo scientifico: “Il percorso didattico comprenderà le conoscenze sviluppate nel XX secolo relative al microcosmo e al macrocosmo, accostando le problematiche che storicamente hanno portato ai nuovi concetti di spazio e tempo, massa ed energia”.
Non credo, tuttavia, che allo studente liceale degli anni precedenti al quinto possa essere evitato completamente il contatto con la meccanica quantistica. Quest’idea è supportata, come abbiamo visto, dalle indicazioni ministeriali per Scienze Naturali, ma anche e soprattutto dall’idea che, senza un approccio quantistico nel secondo biennio del Liceo da parte degli insegnanti di Scienze Naturali, lo studio del mondo molecolare risulta monco. Per esempio, sarebbe difficile, e solamente mnemonico, andare a parlare di “doppietti elettronici” per prevedere la forma delle molecole, anche con approcci semplici come quelli della VSEPR, se non ci fosse alle spalle un’introduzione alla meccanica quantistica. Non credo, infatti, che l’insegnamento della chimica si possa “spogliare” degli aspetti quantistici, delegandoli alla fisica. La fisica, infatti, sia per sua natura disciplinare sia per la preparazione universitaria dei suoi insegnanti (a maggior ragione di quelli laureati in matematica) non si occupa molto di molecole e introduce aspetti quantistici solo per la radiazione elettromagnetica e al massimo per gli atomi.
Vi è, infine, un altro problema generale. Alcuni ritengono che, se non è possibile sviluppare un concetto scientifico in una rigorosa trattazione matematica, è meglio non trattarlo. Seguendo questa linea di pensiero, si potrebbe fare ben poco di meccanica quantistica anche nei corsi generali universitari (per esempio, in Chimica Generale del primo anno). Io non credo all’idea che un concetto scientifico in ambito didattico non possa essere “capito” senza una rigorosa formalizzazione. Prima e dietro alla formalizzazione di un concetto scientifico per lo studente deve, infatti, esserci una “visualizzazione” modellistica, una contestualizzazione nelle problematiche scientifiche e, infine, per i concetti scientifici più importanti che hanno travalicato l’ambito disciplinare, una contestualizzazione culturale fuori dell’ambito scientifico. Sono queste le principali competenze che le discipline scientifiche devono dare del mondo atomico/molecolare allo studente di oggi, cittadino di domani.
In conclusione, possiamo riassumere gli aspetti essenziali analizzati del rapporto della meccanica quantistica con la tradizione chimica e nell’analisi delle problematiche generali della didattica di questi argomenti.
Nel presente contributo e in altri lavori [3, 4] ho cercato di mostrare che l’impostazione generale della chimica e della meccanica quantistica sono differenti. La chimica si propone di padroneggiare un mondo complesso di milioni di sostanze differenti nel piano macroscopico e un mondo molecolare altrettanto complesso a livello microscopico. La strategia utilizzata è quella di raggruppare le sostanze/molecole in categorie che identificano delle caratteristiche essenziali comuni sia statiche (proprietà), collegate alla struttura molecolare, sia dinamiche (reattività), collegate alla variazione nel tempo della struttura molecolare [5, 6]. In particolare, nell’ottica chimica microscopica è essenziale determinare l’organizzazione delle interazioni interatomiche e in particolare “chi è legato a chi”. Il concetto di legame chimico diventa, quindi, il cardine della strutturazione dell’edificio molecolare e della sua trasformazione nelle reazioni chimiche [4].
La meccanica quantistica applicata al mondo molecolare può svolgere una funzione importante nel determinare se una particolare struttura sia stabile e in quali particolari stati; nel determinare i movimenti vincolati della struttura molecolare (roto-vibrazioni), con la possibilità di partire da questi per analizzare il percorso reattivo che modifica lo stato globale del sistema. In quest’ottica globale della molecola, i suoi componenti non sono essenziali e le loro caratteristiche in situ e le loro modifiche nel processo reattivo si possono ritrovare a posteriori per proiezione dalle caratteristiche globali.
Un discorso aggiuntivo va fatto per il concetto di meccanismo di reazione. Qui, la “strutturazione interna” degli enti entra in competizione con la strutturazione tra gli enti per rendere possibile l’atto reattivo. Con questo intendiamo dire che, oltre alla disposizione spaziale degli atomi nelle molecole, è la disposizione delle molecole (e dei relativi atomi) tra di loro a rendere possibile l’atto reattivo. Tale disposizione intermolecolare viene trattata dalla meccanica quantistica solo per reazioni che implicano molecole molto semplici. Spesso si preferisce sviluppare questo aspetto intermolecolare con simulazioni di meccanica classica e, una volta identificata una distribuzione specifica delle molecole, fare per questa il calcolo quantomeccanico. Abbiamo poi accennato alle problematiche sul concetto di meccanismo [7-9], ma il suo rapporto con la meccanica quantistica è ad oggi quasi tutto da indagare. Infine, nel caso delle macromolecole, il meccanismo di reazione ritorna del tutto “interno” all’ente in gioco, alla struttura interna della macromolecola, identificando specifiche sue parti come sito di reazione e/o allosterico. La componente “esterna”, la molecola che si lega al sito allosterico, agisce da “stimolo” (specie attivante) o da repressore (specie disattivante) per il processo reattivo che avviene nel sito di reazione.
Riguardo agli aspetti didattici della meccanica quantistica, possiamo dire che il mondo atomico/molecolare è una risorsa importante per il docente di Scienze Naturali e di Fisica, una risorsa utile sia sul piano motivazionale, perché permette al docente di parlare di “cose attuali”, sia per gli stretti intrecci che tali argomenti consentono con le altre discipline scolastiche. Una risorsa a patto di non introdurlo troppo presto (primo biennio) e, soprattutto, di trattarlo in maniera generale e non esclusivamente formale. Non serve, infatti, una “testa riempita di molecole” (Figure 3), ma una comprensione del perché introduciamo un piano molecolare tra quello atomico e quello macroscopico.

Figura 3. Una testa “riempita” di molecole
Infine, per affrontare in maniera sistematica le sfide educative nell’insegnamento della meccanica quantistica a livello di scuola superiore, i ricercatori sottolineano la necessità di adattare i curricula, di utilizzare la tecnologia e di applicare strategie didattiche innovative che semplifichino la natura astratta della meccanica quantistica, rendendola più accessibile. Inoltre, anche una formazione specifica degli insegnanti [30] è fondamentale per migliorare la comprensione della meccanica quantistica agli studenti e superare le loro convinzioni intuitive che spesso in quest’ambito si rivelano errate.
[1] M. P. Banchetti-Robino, G. Villani, From the Atom to Living Systems. A Chemical and Philosophical Journey into Modern and Contemporary Science, Oxford University Press, New York, 2023, pp. 55-59.
[2] E. Ghibaudi, L. Cerruti, G. Villani, Structure, shape, topology: entangled concepts in molecular chemistry, Foundations of Chemistry, 2020, 22, 279-307.
[3] G. Villani, M. V. Cubellis, Overview of the complex but fruitful relationship between molecular chemistry and quantum mechanics, in celebration of the Year of Quantum Sciences and Technologies, Top Italian Scientists Journal, 2025, 2(4) (https://www.doi.org/10.62684/JDPO8893).
[4] O. Lombardi, G. Villani, About the concept of molecular structure, Foundations of Science, 2024 (https://doi.org/10.1007/s10699-024-09963-y).
[5] G. Villani, La chiave del mondo. Dalla filosofia alla scienza: l’onnipotenza delle molecole, CUEN, Napoli, 2001, pp. 129-144.
[6] G. Villani, Complesso e organizzato. Sistemi strutturati in fisica, chimica, biologia ed oltre, FrancoAngeli, Milano, 2008, pp. 58-62.
[7] P. Machamer, L. Darden, C. Craver, Thinking about mechanisms, Philosophy of Science, 2000, 67, 1-25.
[8] W. Bechtel, Mechanism and Biological Explanation, Philosophy of Science, 2011, 78, 533-557.
[9] R. F. Hendry, Mechanisms in Chemistry, in New Mechanism. Explanation, Emergence and Reduction, J. L. Cordovil, G. Santos, D. Vecchi, D. (Eds.), Cham:Springer, 2023, 35, 139-160.
[10] R. Marcelin, Contribution a l’étude de la cinétique physico-chimique. Annales de Physique, 1915, 9(3), 120-231.
[11] H. Eyring, The activated complex in chemical reactions, Journal of Chemical Physics, 1935, 3, 107-115.
[12] M. G. Evans, M. Polanyi, Further considerations on the thermodynamics of chemical equilibria and reaction rates, Trans. Faraday Soc., 1936, 32, 1333-1360.
[13] M. G. Evans, M. Polanyi, Inertia and driving force of chemical reactions, Trans. Faraday Soc., 1938, 34, 11-24.
[14] H. Eyring, Men, mines, and molecules, Annual Review of Physical Chemistry, 1977, 28, 1-15.
[15] M. C. Gupta, Statistical thermodynamics, New Age International Publishers, New Delhi, 2007.
[16] S. G. Christov, Historical Introduction, in Collision Theory and Statistical Theory of Chemical Reactions, Lecture Notes in Chemistry, Springer, Berlin, Vol. 18, 1980.
[17] J. O. Hirshfelder, E. Wigner, Some quantum‐mechanical considerations in the theory of reactions involving an activation energy, J. Chem. Phys., 1939, 7, 616-628.
[18] G. Villani, A time-dependent quantum approach to allostery and a comparison with light-harvesting in photosynthetic phenomenon, Frontiers in Molecular Biosciences, 2020, 7 (https://doi.org/10.3389/FMOLB.2020.00156).
[19] R. Blonder, et al., Teaching quantum mechanics concepts through problem solving, Physics Education, 2014, 49(2), 208-213.
[20] P. R. L. Heron, et al., Quantum mechanics and the role of interpretation in high school education, Physics Education, 2017, 52(6), 065004.
[21] H. Friedrich, G. Holton, Teaching quantum mechanics at the high school level, Journal of Physics Education, 2003, 42(2), 81-84.
[22] A. Lurio, Teaching quantum mechanics: challenges and innovations, Physics Education, 2001, 36(1), 9-12.
[23] R. Chabay, B. Sherwood, Quantum mechanics: A new approach for teaching and learning, Physics Education, 2010, 45(5), 474-481.
[24] G. Villani, Studiare gli atomi e le molecole nei licei. Alcune considerazioni generali, Nuova Secondaria, 2020, XXXVIII(2), 42-45.
[25] U. Cosentino, M. Venanzi, Percorsi didattici di introduzione alla Meccanica Quantistica, in I tanti volti della chimica. Percorsi innovativi per insegnarla e comprenderla (a cura di E. Aquilini, E. Ghibaudi, M. Venturi, G. Villani), CLUEB, Bologna, 2024, pp. 323-351.
[26] D. Wick, D. Finkelstein, Using interactive simulations to teach quantum mechanics, International Journal of Quantum Chemistry, 2015, 115(6), 369-377.
[27] D. Smith, R. Hemmings, Exploring quantum mechanics through virtual labs and simulations, Journal of Educational Technology Systems, 2020, 49(4), 483-501.
[28] C. A. L. Mahunyag, et al., ELQUAN: A game-based learning tool to master electron configuration and quantum numbers, Journal of Chemical Education, 2025, 102(1), 444-451.
[29] E. Ghibaudi, G. Villani, L’approccio scientifico alla realtà: una riflessione epistemologica, in I tanti volti della chimica. Percorsi innovativi per insegnarla e comprenderla (a cura di E. Aquilini, E. Ghibaudi, M. Venturi, G. Villani), Bologna, 2024, CLUEB, Bologna, 2024, pp. 23-36.
[30] T. Traube, R. Blonder, A computational chemistry course for teachers: From research laboratories to high-school chemistry teaching, Journal of Chemical Education, 2023, 100(11), 4360-4368.
1 Tutte le teorie chimiche quantistiche, alcune esplicitamente e altre implicitamente, si pongono la problematica di trasformare le proprietà molecolari in proprietà atomiche. Teorie come QTAIM (Quantum Theory of Atoms in Molecules) ne sono un chiaro ed evidente esempio. Per un’introduzione a questa teoria si veda https://application.wiley-vch.de/books/sample/3527307486_c01.pdf.
2 Lo “spazio delle configurazione” è uno spazio vettoriale generato dalle coordinate generalizzate che descrivono un insieme di punti qi, i=1, …, nell’interno del quale sono determinate univocamente tutte le loro posizioni. Esso è ben noto ai fisici essendo uno dei concetti essenziali della meccanica razionale, studiata in tutti i Corsi di Laurea in Fisica. Forse non è altrettanto noto ai chimici. Una sua trattazione semplice si trova in un qualunque libro di Meccanica Razionale. In rete, può essere recupoerata negli appunti universitari di tali corsi, come, per esempio, in Appunti dalle Lezioni di Meccanica Razionale tenute dal prof. Raffaele Esposito – Università degli Studi dell’Aquila, https://people.disim.univaq.it/~serva/teaching/Esposito.pdf.