Estrazione e studio della ficocianina da Spirulina platensis: un’esperienza di didattica laboratoriale
Anna Maria Madaio
IIS “B. Focaccia” Salerno
e-mail: annamariamadaio@libero.it
Indice
2. Organizzazione dell’attività
4. Sperimentazione in laboratorio
5. Saggi sulla ficocianina commerciale
6. Purificazione della ficocianina nell’estratto acquoso
Abstract. Phycocyanin, extracted from the cyanobacterium Spirulina platensis, is a phycobiliprotein pigment known for its antioxidant properties and for its use as a natural colorant in the nutraceutical and cosmetic fields. This work describes an experimental pathway carried out by students of a technical institute with a specialization in “Chemistry and Materials,” aimed at studying the characteristics of cyanobacteria and the stages of extraction, purification, and characterization of phycocyanin, as well as the investigation of its denaturation induced by chemical agents. The experience provided students with a comprehensive educational pathway, promoting active learning and problem-solving skills, and promoting the development of competencies in autonomous management of experimental work, critical interpretation of data, and understanding of the relationship between protein structure, stability, and function.
Keywords:Spirulina; ficocianina; denaturazione; spettroscopia UV-Vis; tetrapirrolo, ficobiliproteine
I cianobatteri sono organismi fotoautotrofi che sfruttano la fotosintesi per produrre sostanze organiche grazie a un complesso multiproteico di captazione della luce, il ficobilisoma, localizzato sulle membrane tilacoidali e costituito da pile ordinate di ficobiliproteine, una famiglia di proteine pigmentate in grado di catturare l’energia luminosa e trasferirla alla clorofilla a del fotosistema II.
Le ficobiliproteine sono proteine coniugate legate covalentemente a cromofori tetrapirrolici, detti ficobiline, responsabili della loro fluorescenza e della capacità di assorbimento nella regione del visibile compresa tra 450 e 655 nm, intervallo in cui le clorofille mostrano un assorbimento limitato.
Queste proteine, idrosolubili e dai colori intensi e brillanti, sono costituite da più catene polipeptidiche associate in complessi multimerici. In base alle loro caratteristiche strutturali e spettrali, si distinguono le tre principali classi di ficobiliproteine sotto riportate [1-2].
• Ficoeritrina – esamerica: assorbanza con λmax = 540-570 nm; fluorescenza con λ max = 575-590 nm, colore rosso
• Ficocianina – esamerica: assorbanza con λmax = 610-620 nm; fluorescenza con λ max = 645-653 nm, colore blu
• Alloficocianina – trimerica: assorbanza con λ max = 650-655 nm; fluorescenza con λ max = 657-660 nm, colore azzurro-blu
In questa attività gli studenti hanno sperimentato le tecniche di estrazione e purificazione della ficocianina dal cianobatterio Spirulina platensis e hanno osservato direttamente la relazione tra struttura e funzione della proteina, verificando come l’azione di agenti chimici che interferiscono con i legami intermolecolari, ne provochi la denaturazione e la variazione di alcune proprietà, quali colore e fluorescenza. Contemporaneamente gli studenti hanno approfondito la storia e le caratteristiche biologiche della Spirulina, utilizzata fin dall’antichità come fonte alimentare dagli Aztechi e da popolazioni africane, e oggi coltivata in modo controllato per scopi nutraceutici, cosmetici e, in parte, farmaceutici, grazie al suo elevato contenuto proteico e alla presenza di pigmenti antiossidanti come la ficocianina.
L’attività è stata realizzata in una classe quinta di un istituto tecnico, indirizzo Chimica, Materiali e Biotecnologie, con articolazione Chimica e Materiali, ma può essere facilmente adattata anche ad altri contesti scolastici di tipo tecnico-scientifico. Per lo svolgimento delle attività sono stati necessari alcuni prerequisiti teorici, tra cui la conoscenza della struttura della cellula procariotica, dei processi e pigmenti fotosintetici, della struttura e delle proprietà delle proteine, nonché dei principi fondamentali della spettroscopia UV-Visibile. Le discipline coinvolte sono state Chimica Organica e Biochimica, Analisi Chimica Strumentale, Tecnologie Chimiche Industriali e Storia, allo scopo di favorire un approccio interdisciplinare allo studio della materia vivente e della sua composizione chimica.
Il percorso didattico è stato impostato come un progetto di ricerca sperimentale basato sulla metodologia del problem solving. Gli studenti, anziché seguire una procedura predefinita, hanno costruito progressivamente la metodica sperimentale attraverso una serie di prove pianificate, eseguite e verificate, confrontandosi con il docente, che ha avuto il ruolo di facilitatore del loro processo di apprendimento.
Questo approccio li ha resi protagonisti attivi dell’esperienza, stimolando autonomia, spirito critico e capacità di analisi dei risultati, nonché la ricerca di soluzioni ai problemi emersi durante le fasi sperimentali.
2. Organizzazione dell’attività
L’attività è stata articolata in fasi successive, con un percorso che ha combinato momenti di ricerca, sperimentazione e riflessione critica.
La fase introduttiva, concepita come stimolo per gli studenti e per inquadrare il contesto, ha previsto lo studio autonomo dell’articolo “A Simple Protein Purification and Folding Experiment for General Chemistry Laboratory” pubblicato sul Journal of Chemical Education [3], accompagnato dalla ricerca sul web di ulteriori informazioni sulle proprietà chimico-fisiche della ficocianina [4] e sulla storia, proprietà e modalità di coltivazione della Spirulina platensis [5-10].
A questa fase è seguito un brainstorming in classe, finalizzato all’approfondimento teorico, alla condivisione delle informazioni raccolte, alla ricerca di ulteriore materiale scientifico e alla pianificazione dell’attività sperimentale, successivamente ripartita tra diversi gruppi di studenti.
L’attività didattica si è sviluppata in due fasi principali, strettamente interconnesse l’una all’altra:
• Ricerca e pianificazione - Gli studenti, organizzati in gruppi, hanno ricercato e studiato la letteratura scientifica su Spirulina platensis e ficocianina, elaborando protocolli sperimentali basati su tecniche di estrazione, purificazione e analisi della denaturazione proteica.
• Sperimentazione in laboratorio - In tre lezioni di laboratorio di due ore ciascuna, i gruppi hanno condotto gli esperimenti applicando i protocolli progettati, osservando le variazioni cromatiche e di fluorescenza della ficocianina in diverse condizioni di denaturazione e registrando i dati. Successivamente, durante tre lezioni teoriche di un’ora ciascuna, i dati raccolti sono stati analizzati, confrontati e interpretati, anche in relazione ai risultati riportati in letteratura.
Dopo ogni prova di laboratorio, gli studenti hanno redatto un report giornaliero dei dati acquisiti, seguito da momenti di confronto e analisi critica, per valutare l’efficacia delle procedure e individuare possibili miglioramenti metodologici.
Di seguito sono presentati i risultati finali delle varie fasi, al fine di descrivere in modo completo l’attività svolta e le evidenze emerse.
3.1 Spirulina platensis: storia, proprietà e coltivazione
La Spirulina platensis è un cianobatterio presente sulla Terra da oltre 3,5 miliardi di anni, composto da singole cellule di forma cilindrica (3-12 μ m di diametro), impilate l’una sull’altra a formare lunghi filamenti (detti tricomi), come riportato in figura 1.
È un microrganismo alcalofilo che cresce in ambienti con pH tra 9 e 11, in acque calde, con temperature ottimali di circa 30-35 °C, e in presenza di elevata salinità, tipicamente superiore a 10 g/L di sali totali, condizioni che riducono la competizione microbica e favoriscono la sua dominanza negli habitat naturali.
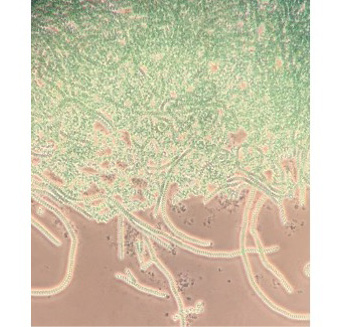
Figura 1. Spirulina Platensis, osservazione al microscopio ottico
I pigmenti fotosintetici di Spirulina platensis sono ficobiliproteine (ficocianina e alloficocianina) e carotenoidi ( β -carotene, criptoxantina, clorofilla a). Tra questi, la ficocianina è la più abbondante ed è caratterizzata da un colore blu brillante e da una fluorescenza rossa. Grazie alla sua straordinaria capacità fotosintetica e alla resistenza a condizioni ambientali estreme, la Spirulina ha svolto un ruolo cruciale nell’evoluzione della Terra, contribuendo alla colonizzazione del pianeta da parte di nuove forme di vita. A seconda della specie, cresce spontaneamente in laghi alcalini e salmastri delle regioni tropicali e subtropicali dell’Africa, del Messico e dell’India, e viene utilizzata fin dai tempi preistorici come fonte di nutrimento dalle popolazioni locali. Gli Aztechi raccoglievano la biomassa dalle lagune, la essiccavano al Sole e la consumavano da sola o in combinazione con altri alimenti come fonte energetica, tanto da essere soprannominata “oro verde degli Aztechi” o “cibo degli dei”. Bernal Díaz del Castillo, esploratore spagnolo e principale cronista della Conquista del Messico, la descrive così nel suo libro intitolato “The Discovery and Conquest of Mexico”:
I pescatori e altri vendevano dolcetti fatti di qualcosa di simile alla melma, che raccolgono da quella grande laguna. Questi si addensano e si trasformano in torte che hanno un sapore un po’ come il formaggio.
Fin dal IX secolo, la Spirulina platensis viene raccolta lungo le sponde del lago Ciad. Le donne dell’etnia Kanembu prelevano la biomassa dalla superficie dell’acqua, la collocano in grandi cesti e la lasciano essiccare al Sole in buche scavate nella sabbia. Il prodotto essiccato viene poi venduto nei mercati locali, rappresentando una fondamentale fonte di reddito per queste comunità.
La Spirulina è oggi uno degli integratori alimentari più diffusi, molto apprezzata per le sue proprietà nutraceutiche e la potente attività antiossidante. Viene anche utilizzata come alimento iperproteico in contesti estremi, tipo il sostentamento degli astronauti nelle missioni spaziali. La sua composizione chimica è particolarmente ricca: contiene dal 55-70% di proteine, 6-10% di lipidi, circa 20% di carboidrati, minerali (K, Ca, Fe, Mg, Zn, …), vitamine (B1, B12, E, …), fibre, acidi grassi polinsaturi (come l’acido γ-linolenico, omega-6) e pigmenti fotosintetici, quali ficobiline, betacarotene e xantofille. Rispetto ad altri alimenti, la Spirulina rappresenta una fonte proteica eccezionalmente preziosa: 100 g contengono una quantità di proteine superiore a quella presente in alimenti comuni come carne bovina (21%), soia secca (35%), prosciutto crudo (28%) o formaggio Grana Padano (34%) [6-8].
Attualmente, Spirulina platensis viene coltivata in stagni poco profondi, vasche aperte o fotobioreattori tubolari chiusi. Il terreno di coltura è ricco di sali inorganici, con elevata concentrazione di bicarbonato, pH compreso tra 9 e 11 e temperature ottimali tra 30 e 35 °C. La composizione del terreno di coltura varia a seconda del protocollo utilizzato e può includere bicarbonato di sodio, solfato di magnesio, nitrato di potassio, cloruro di calcio, solfato di ferro, urea e altri nutrienti.
Raggiunti i livelli di crescita ottimali, la biomassa di Spirulina viene raccolta e filtrata attraverso filtri da 0,5 micron, al fine di rimuovere la maggior parte dell’acqua, ottenendo una pasta liquida che viene poi pressata meccanicamente per eliminare l’acqua residua. La pasta d’alga viene successivamente estrusa, attraverso macchine trafilatrici, in piccoli filamenti di diametro di circa 1,5 mm, come riportato in figura 2, ed essiccata a basse temperature. Il prodotto finale può essere confezionato come spaghettini, sminuzzato o trasformato in polvere [9-10].

Figura 2. Trafilatura della biomassa di Spirulina platensis
La produzione annua globale di biomassa raggiunge circa 4.500 tonnellate, di cui circa il 50% viene prodotta in Cina.
3.2 Ficocianina: struttura e proprietà chimico-fisiche
La ficocianina (Figura 3) è il principale pigmento ficobiliproteico della Spirulina, rappresenta più del 20% del suo peso secco ed è usata come colorante naturale blu in alternativa ai coloranti artificiali Blu brillante FCF (E133) e Patent Blue V (E131), vietati in alcuni paesi. Ha spiccate proprietà antiossidanti e antinfiammatorie, essendo 40 volte più potente delle vitamine C ed E contro i radicali perossidi e ossigeno-reattivi [8].

Figura 3. Ficocianina, pigmento blu
Il cromoforo tetrapirrolico, legato alla proteina tramite un legame tioetereo, grazie all’estesa coniugazione del suo sistema elettronico è responsabile della caratteristica colorazione azzurra della ficocianina. Per comprendere meglio la struttura della ficocianina, gli studenti hanno consultato il sito di Protein Data Bank, dove è disponibile il modello tridimensionale della proteina [11]. Attraverso questa osservazione, hanno potuto analizzare la struttura secondaria e terziaria della ficocianina, individuare la posizione del cromoforo all’interno della molecola e apprezzare la complessità della sua architettura proteica (Figura 4).
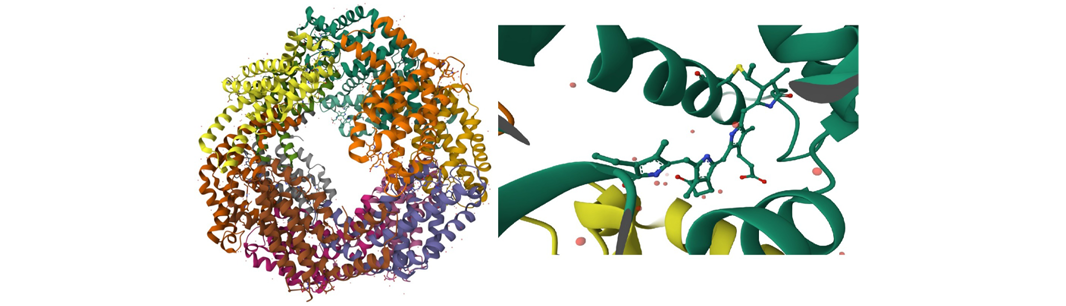
Figura 4. Struttura tridimensionale della ficocianina e cromoforo tetrapirrolico
La ficocianina è altamente sensibile a cambiamenti chimico-fisici e qualsiasi alterazione che agisca sui legami secondari può provocare la perdita della struttura tridimensionale e, di conseguenza, della sua funzione biologica. Lo spettro di assorbimento del cromoforo tetrapirrolico dipende strettamente dalla conformazione della proteina; nella forma nativa, con il cromoforo lineare, la ficocianina assorbe nel visibile a circa 625 nm, conferendo alla proteina il caratteristico colore blu, e mostra una fluorescenza rossa a circa 650 nm. Quando la proteina viene denaturata, il cromoforo assume una conformazione ciclica, assorbe a circa 370 nm, diventando incolore, e perde completamente la fluorescenza [3-4].
4. Sperimentazione in laboratorio
Partendo dalle conoscenze teoriche acquisite sulla struttura e le proprietà della ficocianina, gli studenti hanno potuto comprendere e pianificare i passaggi successivi della sperimentazione. Suddivisi in gruppi, hanno organizzato le attività, implementandole e, quando necessario, perfezionandole in base ai risultati ottenuti. Ad eccezione della prima fase dell’attività sperimentale, relativa all’estrazione della ficocianina e svolta da tutti i gruppi, le altre sono state effettuate da gruppi differenti, mantenendo però un costante confronto e una continua condivisione dei dati tra i partecipanti.
È importante sottolineare che gli studenti non hanno seguito una procedura predefinita, ma hanno ipotizzato , e successivamente perfezionato, la metodica sperimentale seguendo un approccio di tipo problem solving , diventando protagonisti attivi del processo.
Le attività sperimentali inizialmente previste dagli studenti includevano:
• Estrazione della ficocianina da biomassa secca di Spirulina platensis, articolata in varie fasi e svolta da tutti i gruppi
• Saggi di denaturazione dell’estratto acquoso di ficocianina con etanolo e controllo spettrofotometrico
• Saggi di denaturazione dell’estratto acquoso di ficocianina con urea e controllo spettrofotometrico
Sulla base dei risultati ottenuti dalle prime attività sperimentali, gli studenti hanno successivamente elaborato protocolli alternativi utilizzando ficocianina commerciale, con l’obiettivo di sviluppare una metodica di estrazione e analisi della denaturazione facilmente riproducibile.
4.1 Estrazione della ficocianina
Gli studenti hanno sperimentato tre differenti metodologie di estrazione, che hanno portato a estratti acquosi aventi una differente concentrazione di ficocianina.
• Estrazione mediante congelamento-scongelamento: questa tecnica sfrutta la formazione e la rottura dei cristalli di ghiaccio per distruggere le membrane cellulari. Procedimento: 2,5 g di biomassa secca di Spirulina platensis sono stati sospesi in 30,0 mL di acqua distillata, effettuando cicli di congelamento (a –18°C) e scongelamento per 24-48 ore.
• Estrazione mediante lisi meccanica: questa tecnica consiste nel rompere le cellule attraverso l’azione fisica della frantumazione con silice. Procedimento: 2,5 g di biomassa secca di Spirulina platensis e 2,5 g di silice sono stati pestati in un mortaio; la miscela è stata dispersa in 100,0 mL di acqua distillata e conservata a 4°C per una settimana.
• Estrazione mediante ultrasuoni: questa tecnica genera fenomeni di cavitazione che rompono meccanicamente le membrane cellulari. Procedimento: 2,5 g di biomassa secca di Spirulina platensis e 2,5 g di silice sono stati sospesi in 100,0 mL di acqua distillata; la miscela è stata trattata con ultrasuoni per 40 minuti e conservata in frigorifero per una settimana.
Gli estratti acquosi grezzi di colore verde-azzurro scuro sono stati centrifugati a 4000 rpm per 20 min in modo da separare il surnatante blu brillante, contenente la ficocianina, dalla clorofilla e dai residui cellulari (Figura 5).

Figura 5. Separazione del surnatante blu brillante contenente la ficocianina
L’osservazione alla lampada di Wood del surnatante di colore blu ha mostrato la presenza di una fluorescenza viola, e non rossa come descritto in letteratura, visibile anche alla luce solare nelle soluzioni più concentrate (Figura 6) e una fluorescenza azzurra in quelle più diluite.

Figura 6. Surnatante contenente la ficocianina: a) fluorescenza viola alla lampada di Wood; b) fluorescenza viola alla luce solare
Lo spettro visibile dell’estratto acquoso presentava un massimo di assorbimento alla lunghezza d’onda di 618 nm attribuibile alla ficocianina (Figura 7).
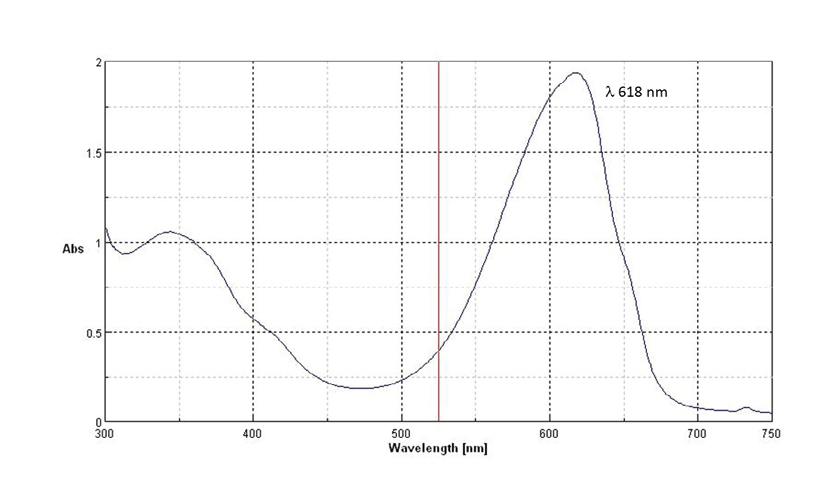
Figura 7. Spettro UV-Vis dell’estratto acquoso di Spirulina platensis
4.2 Saggi di denaturazione dell’estratto acquoso di ficocianina
Sugli estratti acquosi di ficocianina gli studenti, suddivisi in piccoli gruppi, hanno eseguito i saggi di denaturazione per valutare la sensibilità della proteina a vari agenti denaturanti, come etanolo e urea. I saggi sono stati eseguiti su campioni di ficocianina estratta con il metodo di congelamento-scongelamento. I vari risultati sono stati confrontati e razionalizzati, fino ad arrivare a conclusioni condivise.
4.2.1 Denaturazione dell’estratto acquoso di ficocianina con etanolo
L’etanolo è un agente denaturante che agisce riducendo la polarità dell’ambiente e alterando le interazioni idrofile della proteina con l’acqua modificandone la conformazione.
Procedimento: gli studenti, suddivisi in gruppi, hanno preparato diverse diluizioni degli estratti acquosi di ficocianina (1:5, 1:10, 1:25, 1:50) su cui hanno effettuato i vari saggi. Per ogni diluizione sono stati preparati quattro campioni da 2,5 mL, a ciascuno dei quali sono stati aggiunti 2,5 mL di soluzioni di etanolo a concentrazioni crescenti (15%, 30%, 50%, 96%), oltre a un campione di controllo a cui sono stati aggiunti solo 2,5 mL di acqua distillata.
Risultati e Osservazioni
• Per confronto con il controllo, in tutti i campioni con diluizione 1:10 si osservava un evidente cambiamento visivo di colore; in particolare, nel campione con aggiunta di etanolo al 96% si osservava la completa perdita del colore blu, indice dell’avvenuta denaturazione della proteina (Figura 8).
• L’osservazione alla lampada di Wood di tutti i campioni con diluizione 1:10 mostrava la presenza di una persistente fluorescenza azzurra, che nascondeva la graduale scomparsa della fluorescenza viola (Figura 9).
• Per confronto con il controllo, i campioni con diluizione 1:5, denaturati con concentrazioni crescenti di etanolo (15%, 30%, 50%) sono stati analizzati con uno spettrofotometro UV-Vis a doppio raggio per misurare l’andamento dell’assorbanza a 618 nm (tipica della proteina nativa) e a 370 nm (tipica della proteina denaturata). L’aumento della concentrazione di etanolo ha causato, come atteso, una progressiva diminuzione dell’assorbanza a 618 nm, con conseguente diminuzione del colore blu della soluzione, ma anche una diminuzione, e non un aumento, dell’assorbanza a 370 nm (Figura 10).

Figura 8. Campioni di estratto acquoso di ficocianina diluito 1:10 denaturati con etanolo a differente concentrazione; da sinistra verso destra, si nota la progressiva decolorazione all’aumentare della concentrazione di etanolo aggiunto (0%, 15%, 30%, 50%, 96%)
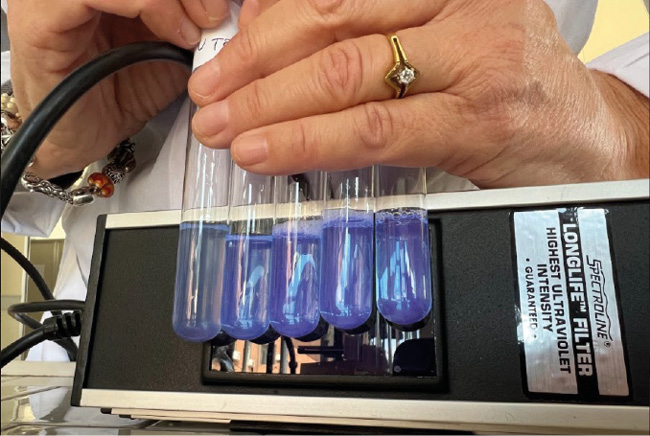
Figura 9. Campioni di estratto acquoso di ficocianina con diluizione 1:10 denaturati con etanolo a differente concentrazione; da destra verso sinistra, si nota la persistente fluorescenza azzurra all’aumentare della concentrazione di etanolo aggiunto (0%, 15%, 30%, 50%, 96%)
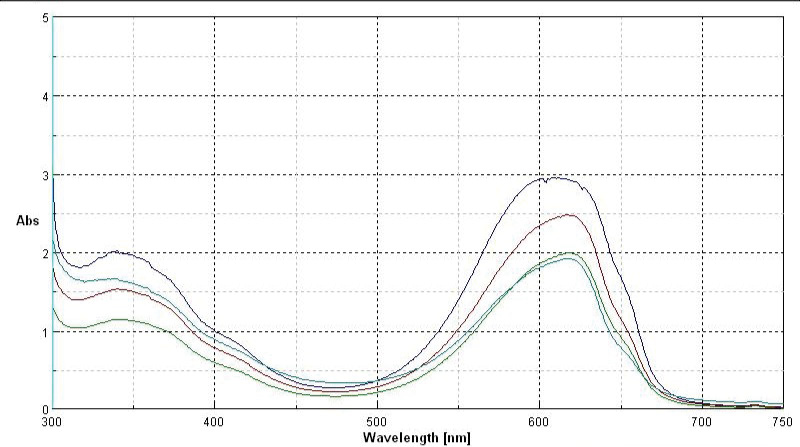
Figura 10. Confronto degli spettri UV-Vis dei campioni di estratto acquoso di ficocianina diluiti 1:5 e denaturati con concentrazioni crescenti di etanolo (0%, 15%, 30%, 50%)
Dall’analisi degli spettri UV-Vis, gli studenti hanno dedotto che il campione utilizzato era molto concentrato e che, per avere risultati attendibili, bisognava diluire ulteriormente le soluzioni. Inoltre, la persistente fluorescenza azzurra nei campioni denaturati faceva pensare alla presenza di impurità nella soluzione.
• Ripetendo la stessa procedura con l’estratto acquoso diluito 1:20 e registrando l’assorbimento con uno spettrofotometro a singolo raggio, gli studenti hanno osservato che, sebbene la denaturazione fosse visibile a occhio nudo come cambiamento di colore, i valori delle assorbanze alla lunghezza d’onda di 618 e di 370 nm erano coerenti con i risultati attesi, ma presentavano variazioni molto piccole e quindi poco attendibili, come mostrato in Tabella 1. Anche in questo caso, si osservava in tutti i campioni una inspiegabile fluorescenza azzurra.
Tabella 1. Valori di assorbanza degli spettri UV-Vis dei campioni di estratto acquoso di ficocianina con diluizione 1:20, denaturati con concentrazioni crescenti di etanolo
|
Campione |
% di etanolo |
Assorbanza (618 nm) |
Assorbanza (370 nm) |
|
1 |
0% |
0,259 |
0,200 |
|
2 |
15% |
0,231 |
0,196 |
|
3 |
30% |
0,219 |
0,206 |
|
4 |
50% |
0,210 |
0,321 |
4.2.2 Denaturazione dell’estratto acquoso di ficocianina con urea
L’urea è un agente denaturante capace di rompere i legami a idrogeno e destabilizzare le strutture secondarie e terziarie delle proteine.
Procedimento: gli studenti hanno preparato quattro campioni contenenti 2,5 mL dell’estratto acquoso di ficocianina senza diluizione, aggiungendo a uno di essi 2,5 mL di acqua (per usarlo come controllo) e agli altri tre, rispettivamente 2,5 mL di soluzioni di urea a concentrazioni differenti (3M, 6M, 8M).
Risultati e osservazioni
• Per confronto con il controllo, solo il campione con aggiunta di urea 8M, pur mantenendo una debole fluorescenza azzurrognola, mostrava segni di denaturazione, con cambiamento di colore da blu a verde-azzurro, ma senza decolorarsi completamente. Gli altri campioni, mantenendo pressoché invariato il colore iniziale, presentavano sempre una fluorescenza viola, visibile anche alla luce solare (Figura 11).

Figura 11. Campioni di estratto acquoso di ficocianina denaturati con soluzioni di urea a concentrazioni crescenti (0M, 3M, 6M, 8M); da destra verso sinistra, all’aumentare della concentrazione di urea, si nota il cambiamento di colore solo nel campione con aggiunta di urea 8M
• Ripetendo le stesse operazioni su campioni di partenza più diluiti, ottenuti aggiungendo 5,0 mL di acqua distillata a tutti i campioni precedentemente preparati, in modo da raggiungere una diluizione 1:2 dell’estratto acquoso, i risultati confermavano la mancata decolorazione delle soluzioni e la persistente fluorescenza viola, visibile anche alla luce del sole (Figura 12).

Figura 12. Campioni di estratto acquoso di ficocianina con diluizione 1:2, denaturati con soluzioni di urea a concentrazioni crescenti (0M, 3M, 6M, 8M), andando da sinistra verso destra
Analizzando i risultati, gli studenti hanno focalizzato la loro attenzione sui due campioni contenenti urea 8M. Nel campione più concentrato, 2,5 mL di estratto acquoso di ficocianina + 2,5 mL di urea 8 M, il colore della soluzione mostrava un cambiamento; in quello più diluito, 2,5 mL di estratto acquoso di ficocianina + 5,0 mL di acqua + 2,5 mL di urea 8 M, il colore della soluzione non cambiava.
Gli studenti hanno, quindi, dedotto l’esistenza di un evidente problema nel rapporto tra la concentrazione dell’agente denaturante e quella della ficocianina nei campioni preparati. In particolare, nel primo caso la concentrazione di ficocianina risultava troppo elevata per la concentrazione di urea utilizzata, con la conseguenza che non tutta la ficocianina veniva denaturata; nel secondo caso la concentrazione di urea presente nel campione non era sufficiente a indurre la denaturazione della ficocianina.
Da un’analisi più attenta dell’articolo scientifico di partenza [3] gli studenti si sono accorti che commettevano un errore nelle aggiunte di urea all’estratto acquoso, perché diluendo un certo volume di urea 8M (2,5 mL) nello stesso volume di soluzione (2,5 mL nel primo caso), o un volume triplo (7,5 mL nel secondo caso), di fatto la concentrazione di urea nel campione diventava rispettivamente la metà (4 M) o un quarto (2 M) di quella iniziale, contrariamente a quanto indicato nell’articolo, che suggeriva una concentrazione di urea 8M nel campione da denaturare.
Questa osservazione ha permesso agli studenti di dare una spiegazione ai risultati ottenuti e di dedurre che, per poter proseguire efficacemente l’attività sperimentale, era necessario focalizzarsi su due fattori critici fondamentali:
• le concentrazioni ottimali dell’estratto acquoso e degli agenti denaturanti necessarie per ottenere risultati coerenti e saggi riproducibili;
• la persistente fluorescenza della ficocianina nonostante la denaturazione della proteina.
Per affrontare questi problemi, si sono resi conto che era fondamentale avere un campione di ficocianina commerciale come riferimento, sia per verificare le caratteristiche di fluorescenza della proteina nativa, sia per la messa a punto dei protocolli di denaturazione e delle successive analisi spettroscopiche.
5. Saggi sulla ficocianina commerciale
Come primo test sulla ficocianina commerciale, gli studenti hanno preparato una sua soluzione a concentrazione non nota e l’hanno osservata alla lampada di Wood. Con grande stupore, hanno verificato che la fluorescenza non era di colore viola, come quella del loro estratto acquoso, ma rossa, in accordo con quanto riportato in letteratura (Figura 13).

Figura 13. Fluorescenza rossa della ficocianina commerciale
Questo risultato suggeriva che la ficocianina estratta in laboratorio non fosse pura e che la fluorescenza viola osservata nell’estratto acquoso fosse probabilmente dovuta alla sovrapposizione della fluorescenza rossa della ficocianina con quella azzurra di altre sostanze presenti nell’estratto acquoso, che rimanevano stabili anche dopo la denaturazione della proteina.
A partire da queste osservazioni, gli studenti, dopo ulteriori attività di brainstorming su dati riportati in letteratura [12-13], hanno elaborato una nuova strategia sperimentale articolata come segue:
• testare i saggi di denaturazione sulla ficocianina commerciale, per individuare le concentrazioni ottimali di proteina e di agenti denaturanti necessarie per ottenere risultati coerenti e riproducibili;
• purificare la ficocianina contenuta nell’estratto acquoso mediante precipitazione con solfato di ammonio, al fine di rimuovere le probabili impurità interferenti;
• confrontare la fluorescenza della ficocianina commerciale con quella della proteina estratta dalla Spirulina platensis e purificata in laboratorio.
5.1 Saggi di denaturazione sulla ficocianina commerciale
Dall’analisi preliminare degli spettri UV-Vis di soluzioni a diversa concentrazione di ficocianina commerciale, gli studenti hanno determinato che la concentrazione ottimale per condurre le prove era pari a 1,0 g/L (Figura 14).
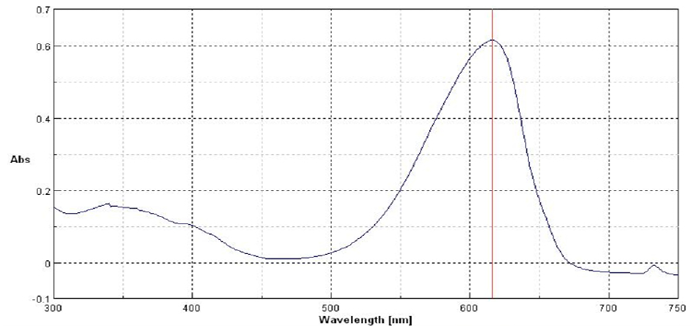
Figura 14. Spettro UV-Vis di una soluzione di ficocianina commerciale 1,0 g/L
Successivamente, hanno pianificato una serie di saggi di denaturazione in presenza di etanolo e urea, preparando campioni di soluzioni di ficocianina in etanolo al 25%, 30%, 35%, 40% e 48% e urea 2M, 4M, 6M e 8M.
Per ottenere le concentrazioni desiderate, gli studenti hanno aggiunto nelle provette contenenti la soluzione di ficocianina 1,0 g/L:
• volumi di soluzioni di etanolo a concentrazione doppia rispetto a quella finale da raggiungere per i saggi;
• quantità pesate di urea e calcolate per raggiungere le concentrazioni molari previste per i saggi.
5.1.1 Denaturazione della ficocianina commerciale 1,0 g/L con etanolo
Per verificare l’effetto denaturante dell’etanolo, gli studenti hanno preparato quattro soluzioni di etanolo al 50%, 60%, 70% e 80% e successivamente sei campioni di cui quattro contenenti ciascuno 2,5 mL di soluzione di ficocianina 1,0 g/L e 2,5 mL delle soluzioni di etanolo a differente concentrazione, uno contenente 2,5 mL di ficocianina commerciale e 2,5 mL di etanolo 96% e un’altro contenente 2,5 mL ficocianina commerciale e 2,5 mL di H₂O distillata, da usare come controllo (Tabella 2).
Come previsto, all’aumentare della concentrazione di etanolo le soluzioni hanno mostrato una evidente e progressiva decolorazione, visibile a occhio nudo, indice della perdita della struttura nativa della proteina. L’avvenuta denaturazione è stata inoltre confermata dalla progressiva diminuzione della fluorescenza osservata alla lampada di Wood.
Tabella 2. Campioni di ficocianina commerciale 1,0 g/L preparati per i test di denaturazione con etanolo a concentrazioni crescenti
|
Campione |
Composizione del campione |
Volume totale |
% finale |
|
1 |
2,5 mL Ficocianina + 2,5 mL H₂O distillata |
5,0 mL |
0 % |
|
2 |
2,5 mL Ficocianina + 2,5 mL etanolo 50% |
5,0 mL |
25 % |
|
3 |
2,5 mL Ficocianina + 2,5 mL etanolo 60% |
5,0 mL |
30 % |
|
4 |
2,5 mL Ficocianina + 2,5 mL etanolo 70% |
5,0 mL |
35 % |
|
5 |
2,5 mL Ficocianina + 2,5 mL etanolo 80% |
5,0 mL |
40 % |
|
6 |
2,5 mL Ficocianina + 2,5 mL etanolo 96% |
5,0 mL |
48 % |
Gli spettri UV-Vis registrati con uno spettrofotometro a doppio raggio hanno ulteriormente validato i risultati: si è osservata una riduzione dell’assorbanza a 618 nm (tipica della forma nativa) e un incremento del segnale a 370 nm, coerente con la formazione della specie denaturata (Figura 15), in perfetto accordo con quanto riportato in letteratura [4].
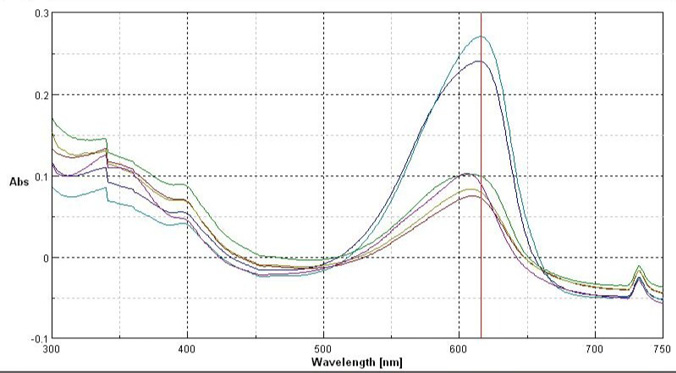
Figura 15. Confronto degli spettri UV-Vis dei campioni di ficocianina commerciale 1,0 g/L denaturati con concentrazioni crescenti di etanolo (0%, 25%, 30%, 48%)
5.1.2 Denaturazione della ficocianina commerciale 1,0 g/L in urea
Analogamente a quanto realizzato nei saggi con etanolo, gli studenti hanno condotto una serie di prove di denaturazione della ficocianina utilizzando urea come agente chimico denaturante.
Sono stati preparati quattro campioni contenenti 5,0 mL di una soluzione di ficocianina commerciale 1,0 g/L, ai quali sono state aggiunte quantità pesate di urea solida, in modo da ottenere le concentrazioni molari finali riportate nella Tabella 3.
Tabella 3. Campioni di ficocianina commerciale 1,0 g/L preparati per i test di denaturazione con urea a concentrazioni crescenti
|
Campioni |
Volume soluzione |
Massa di urea aggiunta |
Concentrazione finale |
|
1 |
5,0 mL |
0,00 g |
0M |
|
2 |
5,0 mL |
0,60 g |
2M |
|
3 |
5,0 mL |
1,20 g |
4M |
|
4 |
5,0 mL |
1,80 g |
6M |
|
5 |
5,0 mL |
2,40 g |
8M |
Per confronto con il campione di controllo, formato solo da 5,0 mL di ficocianina 1,0 g/L, le soluzioni hanno mostrato, come atteso, una progressiva decolorazione all’aumentare della concentrazione di urea, evidenziando la perdita della struttura tridimensionale nativa della proteina (Figura 16).

Figura 16. Campioni di ficocianina commerciale denaturati con urea a differente concentrazione; da sinistra verso destra, si nota la progressiva decolorazione all’aumentare della concentrazione di urea nella soluzione (0M, 2M, 4M, 6M, 8M)
L’osservazione alla lampada di Wood dei campioni ha mostrato la scomparsa graduale della fluorescenza rossa, tipica della ficocianina nativa, senza alcuna comparsa di fluorescenza azzurra, a conferma dell’assenza di altre sostanze fluorescenti interferenti (Figura 17).
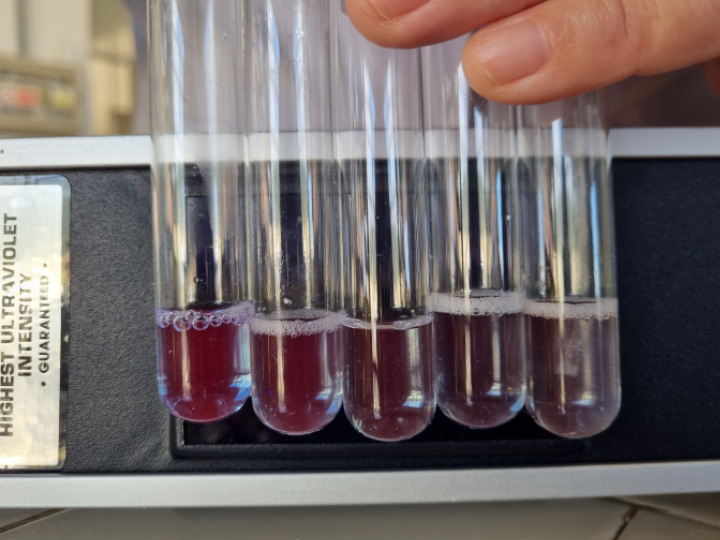
Figura 17. Campioni di ficocianina commerciale denaturati con urea a differente concentrazione; da sinistra verso destra, si nota la progressiva scomparsa della fluorescenza rossa all’aumentare della concentrazione di urea nella soluzione (0M, 2M, 4M, 6M, 8M)
Le misure spettrofotometriche hanno confermato in modo evidente l’effetto denaturante dell’urea, mostrando un andamento analogo a quello osservato nei saggi condotti con etanolo e perfettamente coerente con i dati presenti in letteratura. Gli studenti hanno, quindi, ulteriormente verificato che l’aumento progressivo della concentrazione di urea ha determinato la disgregazione delle strutture secondarie della ficocianina, con conseguente perdita delle sue proprietà ottiche e fluorescenti, evidenziata da una diminuzione dell’assorbanza a 618 nm, tipica della proteina nativa, e da un incremento dell’assorbanza a 370 nm, caratteristica della forma denaturata, come riportato nella Tabella 4.
Tabella 4. Risultati della denaturazione di ficocianina commerciale 1,0 g/L con urea a differenti concentrazioni, confronto tra dati spettroscopici e osservazioni qualitative
|
Campioni |
Molarità urea |
Assorbanza (618 nm) |
Assorbanza (370 nm) |
Osservazioni qualitative (colore e fluorescenza) |
|
1 |
0 (controllo) |
0,820 |
0,110 |
Blu intenso, fluorescenza elevata |
|
2 |
2M |
0,640 |
0,210 |
Blu meno intenso, riduzione fluorescenza |
|
3 |
4M |
0,420 |
0,360 |
Blu pallido, fluorescenza molto ridotta |
|
4 |
6M |
0,250 |
0,520 |
Blu molto pallido, fluorescenza quasi assente |
|
5 |
8M |
0,120 |
0,710 |
Incolore, completa perdita di fluorescenza |
Come risultato dei saggi effettuati sulla ficocianina commerciale, gli studenti hanno individuato le concentrazioni ottimali di proteina da utilizzare nei saggi di denaturazione e hanno definito le condizioni sperimentali più adatte per ottenere risultati coerenti e riproducibili. Inoltre, hanno riconosciuto la necessità di purificare l’estratto acquoso di ficocianina ottenuto da Spirulina platensis , di ripetere su questo campione i saggi di denaturazione già condotti sulla proteina commerciale e di verificare se la fluorescenza azzurra persistente, osservata dopo la denaturazione, fosse causata dalla presenza di impurezze.
6. Purificazione della ficocianina nell’estratto acquoso
Durante la fase di studio e analisi della letteratura scientifica, gli studenti hanno appreso che la solubilità delle proteine varia in funzione della forza ionica della soluzione. A basse concentrazioni saline, la solubilità tende ad aumentare perché gli ioni del sale interagiscono con le regioni polari delle proteine, favorendone la solvatazione (salting in ). Tuttavia, quando la concentrazione salina aumenta in modo significativo (fino a 10-100 volte), le molecole di sale competono con le proteine per le molecole d’acqua, riducendo la loro solvatazione. Di conseguenza, le proteine tendono ad aggregarsi e a precipitare sotto forma di complessi colloidali insolubili (salting out ).
Questa tecnica è comunemente utilizzata per la purificazione selettiva delle proteine senza comprometterne la struttura tridimensionale o la funzionalità biologica.
Per la purificazione della ficocianina contenuta nell’estratto acquoso grezzo, gli studenti hanno utilizzato il solfato di ammonio [12-13], un sale altamente solubile in acqua, capace di generare elevate forze ioniche. Dopo vari tentativi, anche con l’aggiunta diretta di sale solido al campione, sono state individuate le condizioni ottimali per ottenere la precipitazione selettiva della ficocianina.
Procedimento: 20,0 mL di soluzione satura di solfato di ammonio, ottenuta disciogliendo 75,0 g di (NH4)2SO4 in 100,0 mL di acqua distillata, sono stati miscelati con 20,0 mL di estratto acquoso di ficocianina. La miscela è stata lasciata riposare per una notte a 4°C, durante la quale si è avuta la flocculazione del pigmento proteico. Successivamente, il campione è stato centrifugato a 5000 rpm per 20 minuti, ottenendo un precipitato proteico azzurro. Il precipitato è stato risospeso in una soluzione di tampone fosfato a pH 6,8 e il surnatante è stato recuperato (Figura 18).

Figura 18. Fasi della purificazione della ficocianina nell’estratto acquoso: a) flocculazione, b) prodotto della centrifugazione, c) risospensione in tampone fosfato
Risultati e osservazioni
• L’osservazione alla lampada di Wood ha dimostrato che il campione purificato e risospeso in tampone fosfato emetteva fluorescenza rossa, tipica della ficocianina nativa, analogamente al campione di ficocianina commerciale. A dimostrazione della presenza di impurezze fluorescenti, il surnatante recuperato dalla purificazione della ficocianina presentava fluorescenza azzurra (Figura 19).

Figura 19. Confronto, andando da sinistra a destra, tra la fluorescenza viola dell’estratto acquoso di ficocianina, la fluorescenza azzurra del surnatante, la fluorescenza rossa di ficocianina purificata e risospesa nel tampone fosfato e la fluorescenza rossa di ficocianina commerciale
• La misura dello spettro UV-Vis del campione purificato ha evidenziato un picco massimo di assorbanza a circa 618 nm, confermando la presenza della forma nativa della ficocianina (Figura 20).
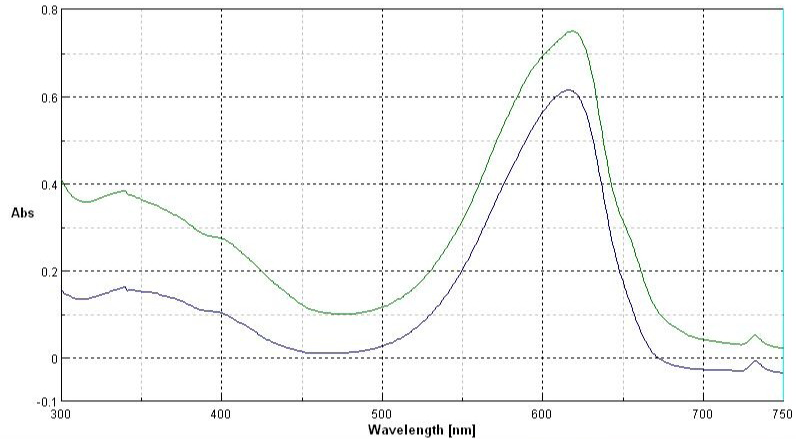
Figura 20. Spettri UV-Vis di ficocianina commerciale (nero) e ficocianina purificata e risospesa in tampone fosfato (verde)
6.1 Saggi di denaturazione sulla ficocianina purificata e risospesa in tampone fosfato
Sulla ficocianina purificata, e risospesa nel tampone fosfato, gli studenti hanno ripetuto i saggi di denaturazione già condotti sulla proteina commerciale, utilizzando le stesse condizioni sperimentali, al fine di verificarne la coerenza e confrontare i cambiamenti visibili di colore e fluorescenza tra le due preparazioni.
Non potendo preparare una soluzione di ficocianina purificata di concentrazione 1,0 g/L, la soluzione tampone contenente la ficocianina è stata diluita fino a ottenere, per quanto possibile, la stessa colorazione della soluzione commerciale di riferimento (1,0 g/L), in modo da poter confrontare direttamente e agevolmente gli effetti dei diversi denaturanti.
Come nelle prove precedenti, la denaturazione con etanolo ha prodotto risultati coerenti con le attese: la soluzione si è progressivamente decolorata e la fluorescenza rossa è diminuita fino a scomparire, esattamente come osservato nella ficocianina commerciale.
Particolare interesse ha suscitato l’osservazione del comportamento della proteina in presenza di urea come agente denaturante. Infatti, come atteso, in soluzione di urea 8M, gli studenti hanno notato una rapida perdita della colorazione blu della ficocianina e la totale scomparsa della fluorescenza rossa, segno dell’avvenuta denaturazione.
In questa fase non sono state effettuate misurazioni spettrofotometriche, dal momento che le evidenze visive raccolte, variazione di colore e scomparsa della fluorescenza, sono risultate sufficienti a confermare l’efficacia del processo e a consentire la stesura di una metodica sperimentale completa e dettagliata per l’intera attività, come riportato in Appendice.
Il confronto tra la ficocianina commerciale e quella purificata in laboratorio ha permesso agli studenti di confermare che:
• la fluorescenza rossa è una proprietà intrinseca della ficocianina nativa
• la fluorescenza azzurra osservata negli estratti acquosi è dovuta a impurezze completamente eliminate con la purificazione mediante salting out
• il processo di precipitazione selettiva con solfato di ammonio è efficace nel separare la ficocianina dalle sostanze interferenti, ottenendo campioni adatti a ulteriori test di denaturazione e analisi spettroscopica.
L’attività di estrazione, purificazione e studio della ficocianina da Spirulina platensis ha rappresentato un’esperienza di grande valore formativo, che ha permesso agli studenti di coniugare conoscenze teoriche, competenze sperimentali e capacità di analisi critica, riproducendo in piccolo le fasi di una vera ricerca scientifica.
Dal punto di vista scientifico, il percorso ha consentito di:
• comprendere la relazione tra struttura e funzione delle proteine, osservando in modo diretto gli effetti della denaturazione sui legami intermolecolari e sulle proprietà cromatiche e fluorescenti della ficocianina;
• verificare l’efficacia del processo di purificazione per salting out con solfato di ammonio, evidenziando la rimozione delle impurezze e la stabilità della proteina nativa;
• osservare le variazioni di colore e fluorescenza come indicatori immediati dello stato conformazionale della proteina, correlando l’esperienza visiva ai concetti di chimica delle proteine e spettroscopia;
• distinguere la fluorescenza rossa caratteristica della ficocianina pura da quella azzurra degli estratti acquosi, dovuta a sostanze accessorie di diversa natura;
• comprendere come la variazione di parametri chimico-fisici (concentrazione salina e presenza di denaturanti) influenzi profondamente la stabilità e le funzioni biologiche di una proteina.
Dal punto di vista didattico, l’attività ha avuto un impatto significativo sul processo di apprendimento:
• gli studenti hanno lavorato in piccoli gruppi, sperimentando il lavoro cooperativo e la pianificazione condivisa delle attività;
• l’approccio basato sul problem solving e sulla ricerca sperimentale ha favorito l’autonomia, la capacità di osservazione e la riflessione critica dei risultati;
• la costruzione progressiva della metodologia, non fornita a priori, ma sviluppata attraverso il confronto e la verifica, ha reso gli studenti protagonisti attivi dell’indagine scientifica;
• la connessione tra teoria e pratica di laboratorio ha consolidato competenze trasversali in Chimica organica, Biochimica e Analisi strumentale, offrendo una visione integrata dei fenomeni biologici e chimici.
Nel complesso, il progetto ha permesso di trasformare un’esperienza di laboratorio in un vero percorso di ricerca didattica, in cui la curiosità e l’osservazione diretta hanno guidato l’apprendimento.
La ficocianina, con le sue variazioni di colore e fluorescenza, si è rivelata non solo un modello efficace per lo studio delle proteine, ma anche uno strumento capace di stimolare l’interesse, la motivazione e la consapevolezza scientifica degli studenti.
Metodica di estrazione e purificazione di ficocianina da Spirulina platensis e studio degli effetti della denaturazione con etanolo e urea
Saggi con ficocianina commerciale 1,0 g/L
Preparare una soluzione 1,0 g/L di ficocianina commerciale, registrare spettro UV-visibile (618 nm e 370 nm) e verificare la presenza di una fluorescenza rossa alla lampada di Wood.
Denaturazione con etanolo
Preparare 4 soluzioni di etanolo al 50%, 60%, 70%, 80%. Verificare la denaturazione in etanolo, preparando 6 campioni di ficocianina commerciale come di seguito indicato:
1) 2,5 mL di ficocianina 1,0 g/L + 2,5 mL di acqua distillata (controllo, 0% etanolo)
2) 2,5 mL di ficocianina 1,0 g/L + 2,5 mL di etanolo 50% (25% etanolo)
3) 2,5 mL di ficocianina 1,0 g/L + 2,5 mL di etanolo 60% (30% etanolo)
4) 2,5 mL di ficocianina 1,0 g/L + 2,5 mL di etanolo 70% (35% etanolo)
5) 2,5 mL di ficocianina 1,0 g/L + 2,5 mL di etanolo 80% (40% etanolo)
6) 2,5 mL di ficocianina 1,0 g/L + 2,5 mL di etanolo 96% (48% etanolo)
Osservare la progressiva decolorazione delle soluzioni e la progressiva scomparsa della fluorescenza rossa, osservabile alla lampada di Wood. Registrare gli spettri UV-visibile dei vari campioni, da cui si nota la diminuzione dell’assorbanza a 625 nm e l’aumento dell’assorbanza a 370 nm.
Denaturazione con urea
Aggiungere urea solida alle soluzioni di ficocianina commerciale 1,0 g/L in modo da ottenere le seguenti molarità di urea nelle soluzioni:
1) 5,0 mL di ficocianina commerciale + 0,60 g di urea (2M di urea)
2) 5,0 mL di ficocianina commerciale + 1,20 g di urea (4M di urea)
3) 5,0 mL di ficocianina commerciale + 1,80 g di urea (6M di urea)
4) 5,0 mL di ficocianina commerciale + 2,40 g di urea (8M di urea)
Osservare la progressiva decolorazione delle soluzioni e la progressiva scomparsa della fluorescenza rossa, osservabile alla lampada di Wood. Registrare gli spettri UV-visibile dei vari campioni, da cui si nota la diminuzione dell’assorbanza a 618 nm e l’aumento dell’assorbanza a 370 nm.
Estrazione di ficocianina da biomassa secca di Spirulina platensis
Lisi cellulare con metodo congelamento-scongelamento
Sospendere 2,5 g di polvere di Spirulina platensis in 30,0 mL di H2O distillata. Effettuare 2/3 cicli di congelamento/scongelamento di 24-48 ore a –18°C.
Centrifugazione dell’estratto acquoso grezzo
Centrifugare l’estratto acquoso grezzo di colore verde scuro a 4000 giri per 20 min per ottenere un surnatante blu brillante, che alla luce del Sole manifesta una fluorescenza viola, e un residuo verde scuro. Prelevare il surnatante contenente la ficocianina per separarlo dal precipitato verde scuro formato dai residui cellulari e clorofilla. Registrare lo spettro UV-visibile dell’estratto acquoso, verificando la presenza del picco di assorbanza a 618 nm.
Purificazione ficocianina dell’estratto acquoso
Precipitazione di ficocianina con soluzione satura di (NH4)2SO4
Sottoporre il campione a un singolo step di precipitazione, usando una soluzione satura di (NH4)2SO4, ottenuta disciogliendo 75 g di (NH4)2SO4 in 100 mL di acqua distillata. Aggiungere 20,0 mL di una soluzione satura di solfato di ammonio a 20,0 mL di estratto acquoso di ficocianina (la flocculazione della proteina avviene quasi immediatamente). Dopo una notte in frigorifero a 4°C, centrifugare la sospensione a 5000 giri per 20 minuti fino a ottenere un surnatante e un residuo proteico. Allontanare il surnatante e verificare la presenza di una fluorescenza blu alla lampada di Wood.
Risospensione in tampone fosfato pH 6,8 del residuo proteico
Risospendere il residuo proteico in una soluzione tampone di fosfato potassico a pH 6,8 (composizione: potassio fosfato monobasico 2,2 g, potassio fosfato bibasico 2,7 g, acqua distillata 500 ml) e verificare alla lampada di Wood la presenza di una fluorescenza rossa, come per la ficocianina commerciale.
Saggi su una soluzione di ficocianina purificata, e risospesa in tampone fosfato, avente lo stesso colore (concentrazione simile) della soluzione 1,0 g/L di ficocianina commerciale
Denaturazione con etanolo
Vedere metodica sopra.
Denaturazione con urea
Vedere metodica sopra.
[1] A. Llopiz, A. Milián, G. Díaz Domínguez, Purification and characterization of phycocyanobilin, Bionatura, 2016, 1(4), 202-207 (https://revistabionatura.com/files/8-Purificacion-y-caracterizacion-de-la-ficocianobilina.pdf).
[2] R. R. Sonani, R. P. Rastogi, R. Patel, D. Madamwar, Recent advances in production, purification and applications of phycobiliproteins, World J. Biol. Chem., 2016 Feb 26; 7 (1), 100-109 (http://dx.doi.org/10.4331/wjbc.v7.i1.100).
[3] R. Bowen, R. Hartung, Y. M. Gindt, A simple protein purification and folding experiment for general chemistry laboratory, J. Chem. Educ., 2000, 77(11), 1456.
[4] B. A. Heller, Y. M. Gindt, A biochemical study of noncovalent forces in proteins using Phycocyanin from Spirulina, J. Chem. Educ., 2000, 77, 1458.
[5] L. Vernès, P. Granvillain, F. Chemat, M. Vian, Phycocyanin from Arthrospira Platensis. production, extraction and analysis, Current Biotechnology, 2015, 4(4), 481-491 (https://www.researchgate.net/publication/285639218_Phycocyanin_from_Arthrospira_Platensis_Production_Extraction_and_Analysis).
[6] M. A. B. Habib, M. Parvin, T. C. Huntington, M. R. Hasan, A review on culture, production and use of Spirulina as food for humans and feeds for domestic animals and fish, FAO Fisheries and Aquaculture Circular No. 1034 (https://www.fao.org/4/i0424e/i0424e00.pdf).
[7] F. Biagioli, Spirulina, perché gli Aztechi la consideravano il nettare degli dei (e ingrediente principale del loro formaggio) (https://www.greenme.it/vivere/salute-e-benessere/spirulina-aztechi/)
[8] C. G. Mila, SPIRULINA, alga azzurra fonte di proteine (https://associazioneargogaudio.org/archivio/90-2013-spirulina,-alga-azzurra-fonte-di-proteine?showall=&limitstart=)
[9] R. Fernandes, J. Campos, M. Serra, J. Fidalgo, H. Almeida, A. Casas, D. Toubarro, A. I. R. N. A. Barros, Exploring the benefits of phycocyanin: from Spirulina cultivation to its widespread applications. Pharmaceuticals, 2023, 16(4), 592 (https://doi.org/10.3390/ph16040592).
[10] E. Gabrielli, G. Stracci, F. Barbato, Ottenimento di ficocianina e misure spettrofotometriche (https://www.algae-event.com/cms/uploads/presentations_2017/7_presentazione_Gabrielli.pdf).
[11] Crystal structure of C-Phycocyanin from Spirulina Platensis, RCSB, Protein Data Bank (https://www.rcsb.org/3d-view/1GH0).
[12] K. C. Duong-Ly, S. B. Gabelli, Chapter Seven - Salting out of Proteins Using Ammonium Sulfate Precipitation, Methods in Enzymology, 2014, 541, 85-94 (https://www.researchgate.net/publication/261183134_Salting_out_of_Proteins_Using_Ammonium_Sulfate_Precipitation).
[13] M. Izadi, M. Fazilati, Extraction and purification of phycocyanin from spirulina platensis and evaluating its antioxidant and anti- inflammatory activity, Asian Journal of Green Chemistry, 2018, 2, 364-379 (https://www.ajgreenchem.com/article_63597_fc7c879d39c89081be2eea96faa9b072.pdf).