Esperimenti didattici
Anna Caronia
Spesso quando si parla di nanoscienze si è convinti che si tratti di argomenti ostici e non sempre facilmente trattabili al biennio o al triennio delle scuole superiori; si pensa inoltre che siano poco connessi ai concetti fondanti della Chimica da inserire in un piano didattico. L’intento del presente contributo è quello di suggerire due semplici attività sperimentali collegabili a diversi concetti fondamentali di questa disciplina quali: miscele; i colloidi e l’effetto Tyndall; l’importanza delle dimensioni collegata alle proprietà fisiche e chimiche della materia; velocità di reazione e catalisi; reazioni di ossidoriduzione; spettroscopia UV-visibile. Gli argomenti possono essere affrontati in modo più o meno approfondito durante il percorso scolastico, ma chiaramente sempre con rigore scientifico. La metodologia applicata nei due percorsi di seguito presentati è quella IBSE, acronimo di Inquiry–Based Science Education , ossia educazione scientifica basata sull’investigazione. Questo approccio pedagogico, come riportato in diversi studi e anche nel Rapporto Rocard 2007, stimola la formulazione di domande e azioni per risolvere problemi e capire fenomeni. Il metodo prevede una sequenza di fasi, basati sul metodo delle così dette 5 E (Engage, Explore, Explain, Elaborate, Evaluate), nella consapevolezza che la pratica didattica dovrebbe essere impostata in modo da “fare scienza” piuttosto che “fare lezione”. Seguendo tale metodologia, gli studenti, in modo naturale si abituano a pensare come gli scienziati: prevedono, spiegano e successivamente validano le ipotesi formulate.
La prima attività che ha come titolo “Il carbone attivo: l’importanza della dimensione”, ha l’obiettivo di far comprendere agli studenti l’importanza della dimensione e del rapporto superficie volume in riferimento alle proprietà di un materiale.
Si può iniziare il percorso con qualche domanda problema (fase Engage): Il carbone attivo cos’è? Per cosa viene usato il carbone attivo vegetale?
Dopo avere compreso assieme agli studenti cosa è il carbone attivo e quali sono le possibili proprietà, si passa alla fase sperimentale e di verifica delle proposte avanzate.
La classe divisa in gruppi discute sulla realizzazione di un esperimento collegato al fenomeno del diverso adsorbimento del carbone attivo di disuguale pezzatura a parità di quantità utilizzata ( fase Explore ). A tal fine, attraverso una semplice attività sperimentale, si studia il fenomeno della decolorazione di una soluzione di acqua e inchiostro in presenza di carbone attivo. Ogni gruppo ha a disposizione la stessa quantità di carbone attivo, ma di diversa granulometria, la stessa soluzione di acqua e inchiostro e devono far sì che il tempo di contatto del carbone attivo con la soluzione sia uguale in ciascun esperimento. È fondamentale, infatti, quando si costruiscono modelli e si verificano ipotesi, studiare una sola variabile alla volta, in questo caso specifico la diversa pezzatura del carbone attivo. Alla fine dell’esperimento i gruppi confrontano l’intensità di colorazione della soluzione che non è uguale per tutti. Dall’analisi dei risultati e dalla discussione emerge che le soluzioni che sono a contatto con il carbone attivo a pezzatura minore si sono decolorate di più in quanto a parità di quantità di carbone la superficie di contatto è maggiore e quindi più grande è la capacità di adsorbimento.
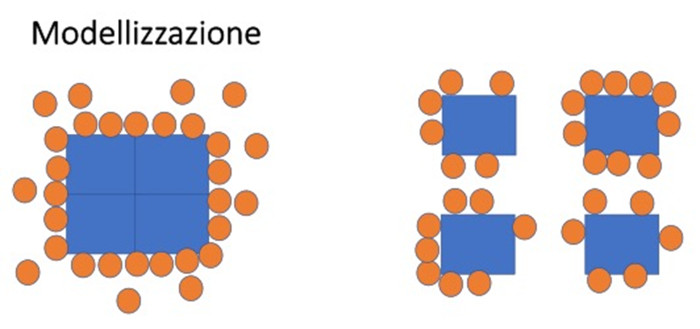
Dopo la fase sperimentale è importante spiegare e passare alla modellizzazione di quanto osservato mettendo in evidenza che le proprietà della materia sono collegate alle dimensioni ed al rapporto superficie volume.
Questo è possibile farlo realizzando un’altra semplice attività: si costruisce un rettangolo grande ottenuto dall’unione di quattro rettangoli tra di loro equivalenti e si hanno a disposizione un certo numero di cerchietti o di tappi di bottiglia.
Quando si avvicinano i cerchietti al rettangolo grande non tutti possono rimanere a diretto contatto della figura geometrica, mentre, se dividiamo il rettangolo in quattro parti, tutti i cerchietti potranno aderire alla superficie del rettangolo.

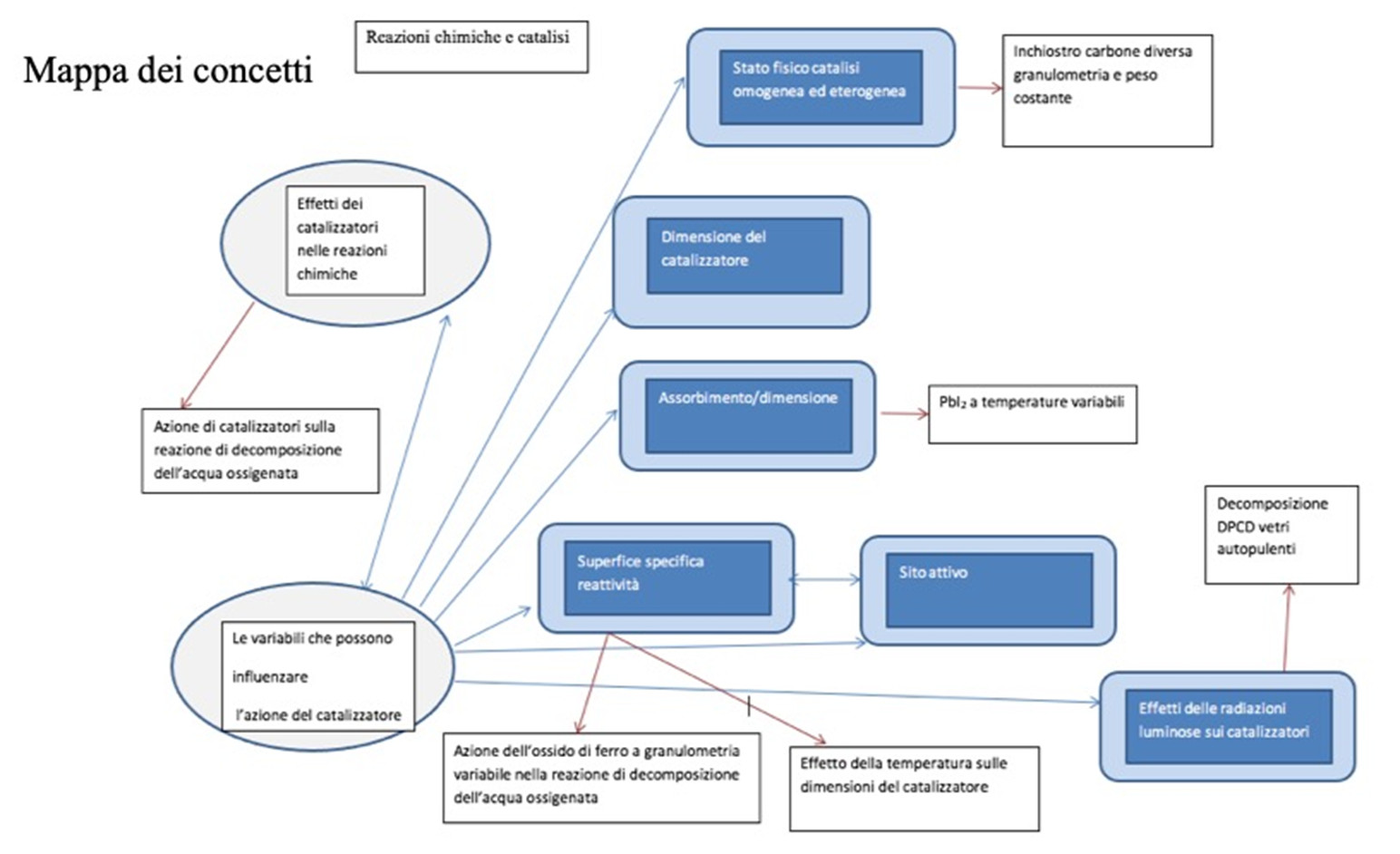
Queste attività sono state sviluppate all’interno di un modulo, del progetto IRRESISTIBLE, che si concentra sulle proprietà dei nanocristalli e dei materiali nanoporosi e sulle loro applicazioni nei processi catalitici utilizzati nella protezione ambientale.
La seconda attività proposta, dal titolo “Nanoparticelle d’argento: sintesi e caratterizzazione”, è stata pensata per un percorso didattico dedicato alle miscele all’interno del quale un’unità formativa può essere dedicata ai colloidi.
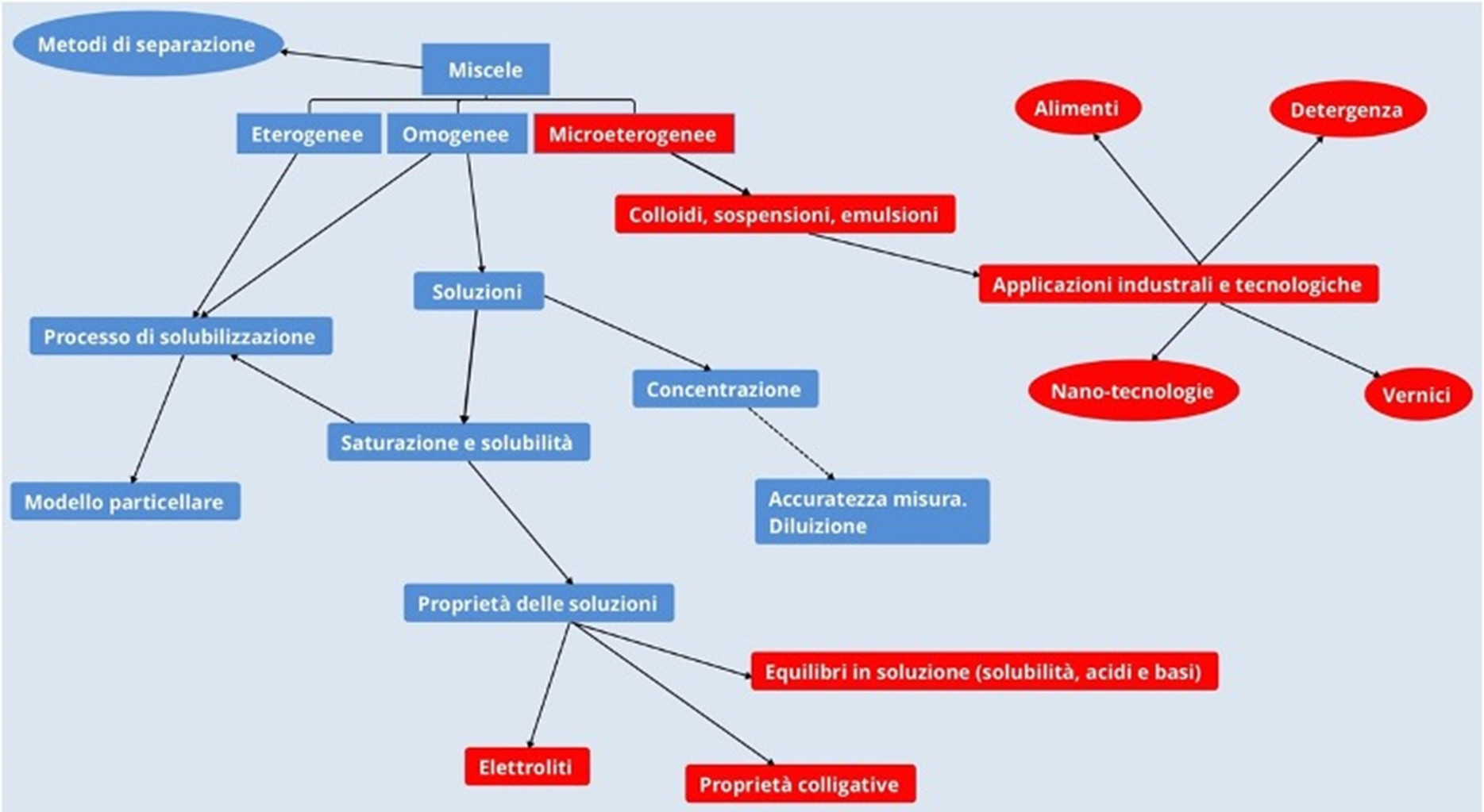
In particolare, facendo riferimento alle miscele, con un esperimento pratico si mette in evidenza la differenza tra sospensioni e colloidi.
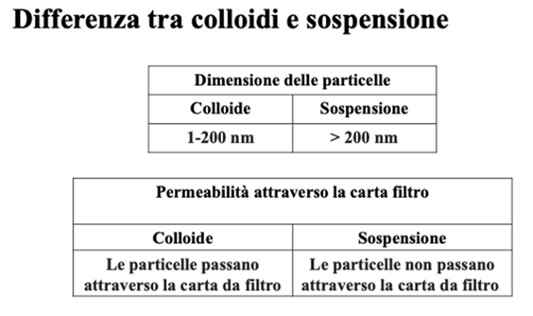
Successivamente si studiano e caratterizzano le sospensioni colloidali, (acqua e latte, gelatina in acqua, amido in acqua) sfruttando l’effetto Tyndall. Per evidenziare tale effetto si può utilizzare un puntatore-laser.
Sperimentalmente avviene che:
Per quanto riguarda le nanotecnologie, un approfondimento sulla chimica dei colloidi può essere effettuato mediante la sintesi di oro o argento nanostrutturato. Nel caso specifico sono state preparate nanoparticelle d’argento (NPAg) perché i reagenti sono più facilmente reperibili e meno costosi, come evidenziato dalla seguente reazione
AgNO3
+ NaBH4
= Ag+ 2H2
+ 2B2
H6
+NaNO3
in cui l’argento, a freddo, viene ridotto utilizzando come riducente, per esempio, il sodio boroidruro.
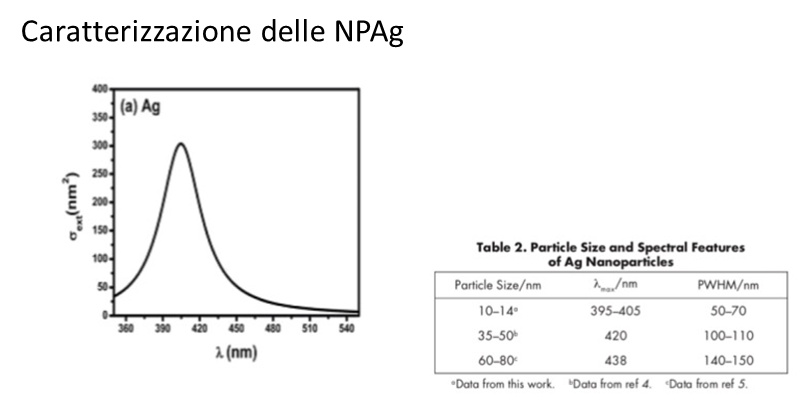
Con questo metodo si ottengono particelle di dimensione di 12 ± 2 nm.
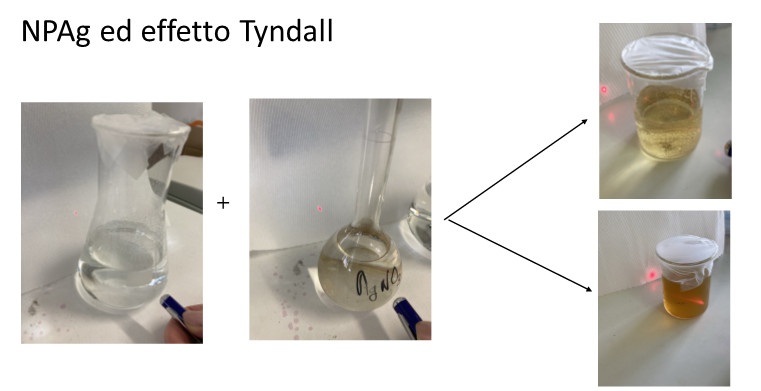
Altro possibile percorso in cui introdurre la sintesi di nanoparticelle è quello dedicato alla spettroscopia UV-visibile, in quanto la loro caratterizzazione viene effettuata tramite analisi spettrofotometrica. Tipico delle nanoparticelle di Ag è il colore giallo dovuto all’interazione della luce con le nanoparticelle che assorbono prevalentemente nella regione del blu (400 nm), colore complementare rispetto al giallo.
Infine, è sicuramente importante mettere in evidenza, quando si affronta lo studio dei sistemi nanostrutturati, la differenza delle proprietà delle sostanze in fase massiva rispetto alle proprietà delle stesse sostanze in sistemi formati da un numero definito di particelle: ciò è conseguenza del fatto che atomi e molecole cambiano comportamento in base al contesto, alle specie vicine, al loro numero e al tipo di interazioni possibili.
M. Rocard, et al., Science Education Now: A Renewed Pedagogy for the Future of Europe , Report EU22-845, Brussels, 2007.
R. W. Bybee, et al., The BSCS 5E Instructional Model: Origins, Effectiveness and Applications , BSCS Colorado Springs, 2006.
The catalytic properties of nanomaterials (Poland):
http://www.irresistible-project.eu/index.php/en/resources/teaching-modules
E-book: Corso di Didattica della Chimica (X Scuola di Didattica e Ricerca
Educativa U. Segre)
https://www.soc.chim.it/sites/default/files/users/sci_didattica/Corso%20di%20Didattica%20della%20Chimica_copertine.pdf
S. D. Solomon, M. Bahadory, A. V. Jeyarajasingam, S. A. Rutkowsky, C. Boritz, L. Mulfinger. Synthesis and Study of Silver Nanoparticles, Journal of Chemical Education , 2007, 84 (2), 322.
Video presentazione
A. Caronia:
https://youtu.be/CtmyZE7vfhw