Nel nome di Elais: dall’olio di oliva agli oli essenziali
Maria Irene Donnoli e Dina Anna Maria Smaldone
IIS “Einstein-De Lorenzo” di Potenza
e-mail: iredon72@gmail.com; dina.smaldone@gmail.com
Indice
2. Caratterizzazione analitica dell’olio di oliva
3. Recupero di oli esausti: il biodiesel
5. Impiego degli oli essenziali
Abstract. This work represents an educational experience included in the PTOF project named “The essential is circular”, which involves extraction of essential oils by natural sources like lavender, rosemary, orange, other citrus fruits and other materials. Most of these sources are partly used for other processes and the unused portion most often constitutes waste. The idea is to turn these potential wastes into resources by implementing the concept of circular economy; in this experience the students develop specific skills using the teaching methodology of Service Learning.
Keywords: olio di oliva; economia circolare; biodiesel; oli essenziali; didattica laboratoriale; Service Learning
Perché il nostro lavoro inizia con il nome di Elais? Secondo la tradizione mitologica, Elais (Ελαϊς, Figura 1), figlia di Aniou e di Dorippe, era la protettrice dell’olio d’oliva.

Figura 1. Elais (Ελαϊς) protettrice dell’olio
Le sue sorelle erano Oino (Οινώ), che proteggeva la vigna, e Spermò (Σπερμώ), che proteggeva il grano. L’olio d’oliva, il vino e il grano sono i tre preziosi prodotti della terra greca. Come per altre popolazioni antiche, la triade grano-vite-ulivo, rappresenta l’unità fondamentale della sopravvivenza civilizzata, perché farina, vino e olio non si trovano in natura, ma sono ottenuti tramite una particolare e sapiente lavorazione. Sin dai tempi antichi l’ulivo è stato l’albero più sacro e fino a oggi rimane un elemento direttamente correlato alla tradizione, ma anche all’alimentazione della Grecia e dei paesi che si affacciano sul Mediterraneo, come il nostro. Il ramo d’ulivo era, inoltre, un simbolo di pace, saggezza e vittoria.
Il nostro lavoro, pertanto, parte dall’olio di oliva per poi considerare anche gli altri tipi di oli come quelli essenziali che portano con loro tanti benefici per il nostro benessere quotidiano.
Con questo progetto ci prefiggiamo di far raggiungere agli allievi delle classi del triennio dell’indirizzo Chimica, Materiali e Biotecnologie dell’IIS Einstein De Lorenzo di Potenza, le competenze necessarie per permettere loro di condurre in autonomia un’analisi completa di caratterizzazione dell’olio di oliva, per valutarne la qualità e determinarne la classificazione. Un ulteriore obiettivo è quello di sviluppare negli studenti una coscienza in tema di eco-sostenibilità ambientale che permetta di ridurre al minimo i materiali di scarto. Le attività laboratoriali sono state progettate per permettere agli studenti di raggiungere competenze tali da saper scegliere le più opportune tecniche di estrazione di oli essenziali da matrici vegetali e da saper comunicare i risultati ottenuti attraverso metodologie didattiche innovative.
2. Caratterizzazione analitica dell’olio di oliva
Per accertare o verificare la qualità, la conservabilità e la genuinità dell’olio di oliva è necessario eseguire analisi chimiche [1] secondo procedure codificate da specifici regolamenti europei (Regolamento CEE n. 2568/91 e successive modifiche).
L’acidità di un olio esprime la percentuale in peso di acidi grassi liberi nel campione in esame (Figura 2).
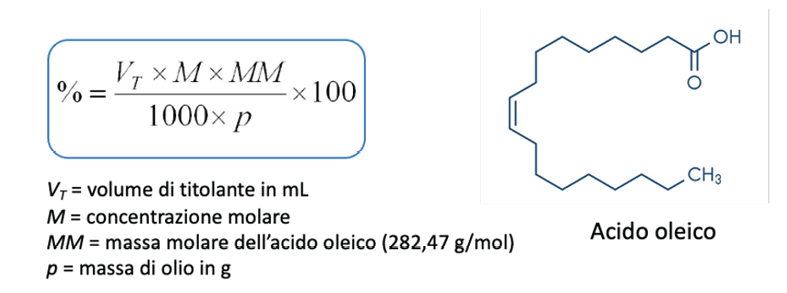
Figura 2. Espressione dell’acidità dell’olio di oliva e struttura dell’acido olieico
Gli acidi grassi sono presenti negli oli come conseguenza della progressiva deacilazione dei trigliceridi, e l’aumento del numero di acidi grassi liberi determina l’incremento dell’acidità libera. Nell’olio di oliva questo è dovuto all’azione di enzimi come le lipasi, naturalmente presenti nel frutto, responsabili dell’idrolisi dei trigliceridi. Lo stesso meccanismo lipolitico può essere causato da enzimi prodotti da microrganismi che crescono sul frutto. L’aumento dell’acidità avviene sia per la conservazione delle olive in fase di pre-molitura, sia a causa dell’invecchiamento dell’olio e quindi aumenta in funzione del tempo di conservazione.
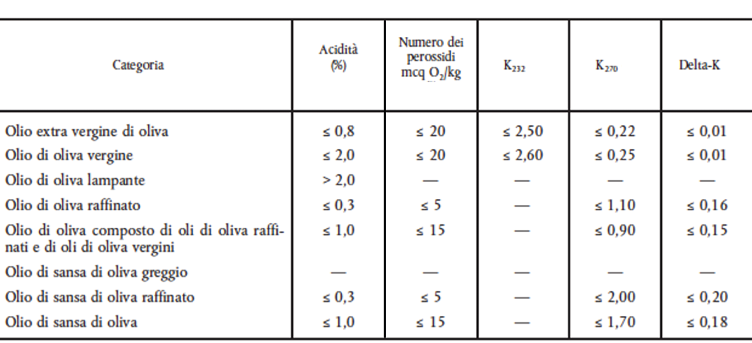
L’acidità di un olio non influenza direttamente le caratteristiche sensoriali del prodotto, ma è un importante indice per la classificazione merceologica del prodotto olio extravergine di oliva (Tabella 1, Regolamento CE 1989/2003).
Tabella 1. Parametri merceologici fondamentali di oli di oliva (Regolamento CE 1989/2003)
L’acidità indica, in un olio nuovo la qualità delle olive, mentre in un olio conservato lo stato di conservazione. Viene determinata attraverso una titolazione acido-base (Figura 3) [2]: ad una quantità nota di olio viene aggiunto un solvente opportuno (lipofilo) e un indicatore acido-base (fenolftaleina). Alla soluzione vengono poi aggiunti volumi noti di KOH a una concentrazione nota. L’indicatore diventa rosa persistente appena tutti gli acidi grassi liberi hanno reagito con il KOH.
A questo punto si calcola la quantità di KOH utilizzata e si risale all’acidità. L’acidità viene espressa come riportato in Figura 2, dove VT è il volume in mL della soluzione di KOH usata; M è la concentrazione della soluzione di KOH; MM è la massa molare dell’acido adottato per l’espressione dei risultati (Acido oleico = 282,47 g/mol); p è il peso in grammi del campione.
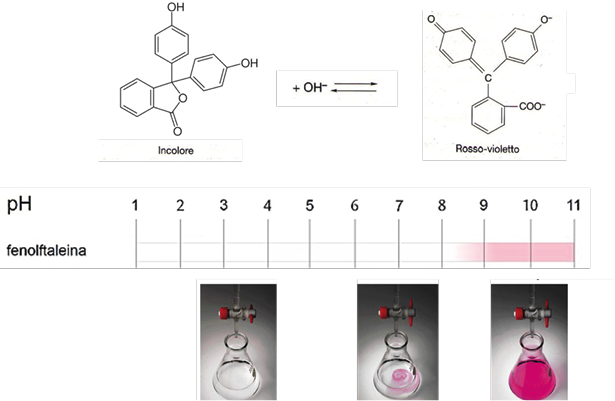
Figura 3. Titolazione acido base, indicatore fenolftaleina
La quantità di ossigeno presente, indicata come numero di perossidi, esprime il livello di alterazione che l’olio ha subito: più alto è il suo valore, più avanzato è lo stato di irrancidimento. Negli acidi grassi insaturi l’ossigeno tende a legarsi facilmente ai carboni impegnati nei doppi legami originando perossidi; questi sono in grado di spostare lo iodio da una soluzione di ioduro (lo iodio viene ossidato e i perossidi si riducono). La quantità di I2 che si libera da questa reazione è direttamente proporzionale alla quantità di idroperossidi presenti nel campione, per cui si può risalire alla loro quantità mediante titolazione con tiosolfato di sodio a concentrazione nota in presenza di salda d’amido (Figura 4). Quest’ultima con lo iodio assume una tipica colorazione blu, quando tutto lo iodio viene titolato tale colorazione scompare. Conoscendo la normalità e i millilitri di tiosolfato usati nella titolazione è possibile calcolare gli equivalenti di iodio spostati dall’ossigeno, che sono quindi uguali a quelli di ossigeno: meq/kg di O2 = V × N × ١٠٠٠ m dove V = volume della soluzione di tiosolfato usato nella titolazione, N = normalità del tiosolfato e m = massa (g) del campione analizzato [3].

Figura 4. Titolazione iodometrica per la determinazione del numero di perossidi nell’olio di oliva
Il numero di perossidi di un olio extravergine in ottimo stato di conservazione è solitamente inferiore a 10 meq/kg di olio, ma per legge deve essere inferiore a 20 meq/kg di olio (Tabella 1).
L’analisi spettrofotometrica dell’olio di oliva nell’ultravioletto (UV) è riportata nell’Allegato IX del Regolamento CEE 2568/91: sono indicati i reagenti necessari, i criteri di qualità della strumentazione e le modalità di espressione dei risultati.
Nell’analisi spettrofotometrica degli oli si determinano i valori di estinzioni specifiche, comunemente indicati con la lettera K. K232 è un parametro che misura l’assorbimento della radiazione UV alla lunghezza d’onda di 232 nm e fornisce informazioni interessanti sull’eventuale modifica della struttura dell’olio in seguito all’ossidazione (Figura 5) [4]. Questo parametro può aumentare anche in caso di olio rettificato. Secondo la normativa vigente il valore massimo per l’olio extra vergine è 2,50.
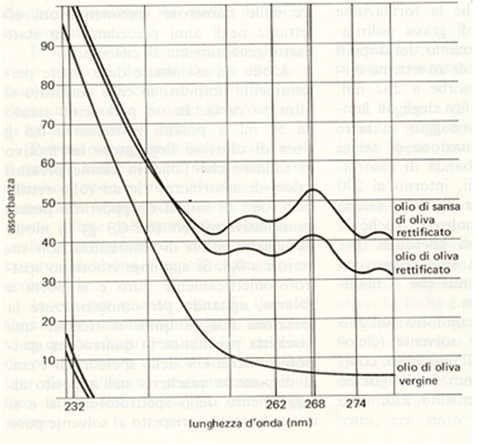
Figura 5. Spettri UV di vari tipi di olio di oliva
K270 (o K268) misura invece l’assorbimento della luce ultravioletta a una lunghezza d’onda di 270 nm (o 268 nm) (Figura 5). In questo caso, viene verificato lo stato di ossidazione secondaria di ciascun modello, ossia le eventuali trasformazioni della struttura dell’olio in seguito alla formazione dei doppi legami. Molto spesso può succedere che vengano generati addirittura tre o quattro doppi legami coniugati, in grado di compromettere il gusto e la qualità dell’olio stesso e di non renderlo più extravergine. Il valore può crescere anche in seguito a una conservazione prolungata. Secondo la normativa vigente il valore massimo per l’olio extra vergine è 0,22.
Il numero di saponificazione o il valore di saponificazione si riferisce al numero di idrossido di potassio o idrossido di sodio richiesto per saponificare un grammo di olio in condizioni specificate. Questo numero è un valore del peso molecolare medio di tutti gli acidi grassi presenti come trigliceridi nel campione di olio. Maggiore è questo valore, minore è la lunghezza media degli acidi grassi e minore è il peso molecolare medio dei trigliceridi. La sua misura è generalmente basata su una retro-titolazione: il campione viene trattato con una quantità nota di soluzione di base certamente in eccesso e scaldandolo a ricadere per almeno un’ora. Al termine dell’ora, dopo raffreddamento, l’eccesso di base che non ha reagito viene misurato per titolazione con una soluzione di acido forte (generalmente acido cloridrico) in presenza di fenolftaleina. La medesima misura viene effettuata su un bianco, del tutto identico al campione, ma non contenente alcun grasso. Il numero di saponificazione si calcola secondo la formula riportata in Figura 6 dove: V è il volume di soluzione di acido cloridrico impiegato nella prova in bianco, espresso in millilitri, V1 è il volume di soluzione di acido cloridrico impiegato nella prova reale, espresso in millilitri, N è la normalità della soluzione di acido cloridrico, Mb è la massa molare della base utilizzata per la saponificazione (56 g/mol per KOH e 40 g/mol per NaOH), e m è la massa del campione prelevato per la determinazione, espressa in grammi.
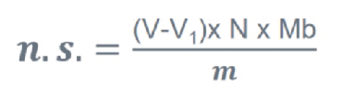
Figura 6. Formula per la determinazione del numero di saponificazione
Nei laboratori didattici del nostro Istituto sono stati analizzati tre diversi campioni di olio di oliva non commerciale, e classificati tutti come oli extravergini di oliva: i dati di caratterizzazione sono riportati nella Tabella 2.
Tabella 2. Parametri di caratterizzazione derivanti dall’analisi di campioni di oli di oliva

3. Recupero di oli esausti: il biodiesel
Nel nostro istituto già da diversi anni si lavora affinché gli studenti acquisiscano competenze di cittadinanza e ne diventino ogni giorno sempre più consapevoli. Le competenze europee alle quali si fa riferimento sono principalmente: competenza personale, sociale e capacità di imparare a imparare; competenza sociale e civica in materia di cittadinanza; competenza imprenditoriale. I goals dell’agenda 2030 che si intende raggiungere sono: 8, 12 e 13.
In questo senso e nell’ottica di un’economia circolare (Figura 7) nasce, già dal 2008 (poi ripreso negli anni scolastici 2020-21 e 2022-23) il progetto di recupero degli oli vegetali esausti, al fine di ottenere combustibili sostenibili di natura non fossile. Gli oli esausti di frittura, recuperati, vengono trasformati in biodiesel per l’ottenimento di biocarburanti.
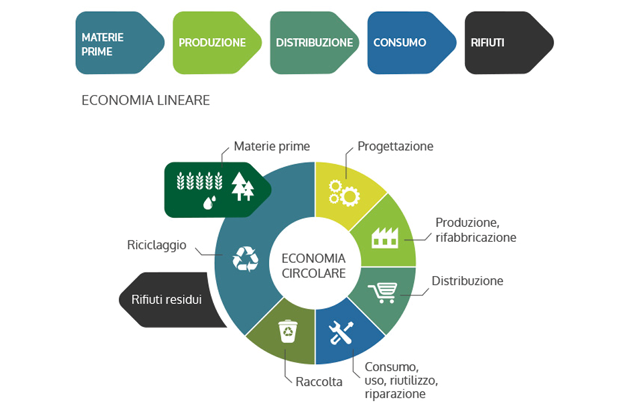
Figura 7. Economia Lineare vs Economia Circolare
Il biodiesel è un combustibile ottenuto da fonti rinnovabili. Esso è ottenuto mediante la reazione di trans-esterificazione che consiste nella rottura degli acidi grassi che caratterizzano gli oli vegetali. Alla fine di questo processo il biodiesel si presenta sotto forma di liquido color ambrato con una viscosità simile a quella del gasolio (Figura 8).

Figura 8. Biodiesel ottenuto nei laboratori didattici dell’IIS “Einstein De Lorenzo” Potenza
Prima di descrivere il processo chimico che porta alla formazione del biodiesel, soffermiamoci su cosa sono gli oli esausti. Gli oli esausti sono oli alimentari che cambiano la propria struttura originaria a seguito di una frittura: si ossidano e assorbono le sostanze inquinanti dalla carbonizzazione dei residui alimentari. Questi scarti hanno una pericolosità molto elevata, che viene spesso ignorata o sottovalutata, se vengono buttati nello scarico; possono, infatti, trasformarsi in potenti agenti inquinanti non biodegradabili, che rendono inutilizzabili i pozzi d’acqua, possono rendere inutile l’azione dei depuratori, impedire alle radici di portare nutrienti alle piante, compromettendo sia la flora che la fauna. Esistono, però, metodi particolari per riciclarli, dal momento che possono essere smaltiti nelle varie isole ecologiche presenti sui territori comunali, o possono essere consegnati ad aziende iscritte al Consorzio Obbligatorio Nazionale di Raccolta e Trattamento Oli e Grassi Vegetali ed Animali Esausti (CONOE).
Il decreto legislativo 27 gennaio 1992 n. 95, “Norme relative alla eliminazione degli oli usati”, è la fonte normativa principale per la raccolta e lo smaltimento degli oli usati, sia di natura privata che industriale. Una volta entrato nel processo di smaltimento, l’olio esausto viene immesso nel mercato sotto forma di altri prodotti come il biodiesel, oppure viene utilizzato per il recupero energetico, oppure da esso si recupera la glicerina in seguito al processo di saponificazione.
Il biodiesel è un combustibile composto da una miscela di esteri alchilici di acidi grassi a lunga catena, che può essere prodotto in modo sostenibile dall’uso di oli vegetali di scarto. Questi oli contengono una maggiore quantità di acidi grassi liberi che si formano nell’olio quando è scaldato ad alte temperature e per un tempo prolungato in presenza dell’acqua rilasciata dagli alimenti durante la cottura. La reazione che provoca la formazione degli acidi è l’idrolisi dei trigliceridi dell’olio; questi, trattati con metanolo in eccesso e in presenza di sodio metossido come catalizzatore basico, si trasformano in esteri metilici degli acidi grassi e glicerolo.
Lo scopo del nostro esperimento è stato proprio quello di ottenere, in quantità limitata, del biodiesel partendo da olio di frittura. Abbiamo deciso di effettuare due esperimenti, con finalità comune, ma con diversi procedimenti, allo scopo di verificare la resa migliore di biodiesel e la sua qualità.
Il primo esperimento prevede una reazione di transesterificazione con idrossido di potassio, mentre il secondo con metossido di sodio (Figura 9).
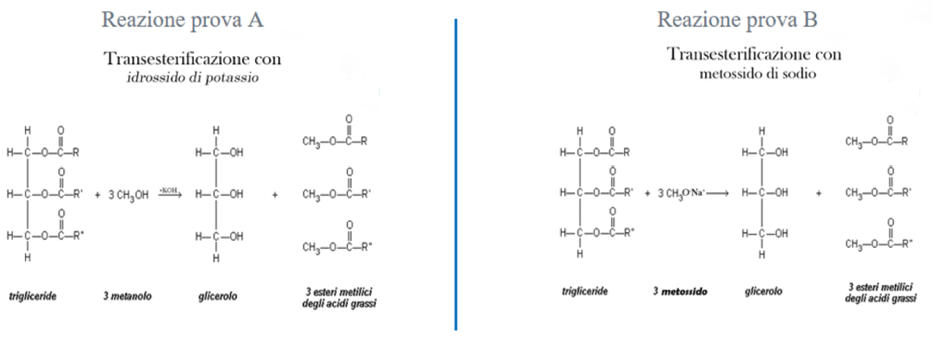
Figura 9. Schema di reazione di transesterificazione di trigliceridi con KOH (prova A) e CH3ONa (prova B) realizzato dagli alunni dell’IIS Einstein De Lorenzo
Il prodotto di reazione viene purificato e valutato. I parametri presi in considerazione sono: la resa di reazione, l’acidità, la densità e i prodotti formati in seguito a combustione. Il biodiesel, rispetto al comune gasolio per autotrazione, presenta diversi vantaggi; infatti, è un prodotto a impatto zero; riduce le emissioni nette di monossido di carbonio (CO) di circa il 50% e di diossido di carbonio (CO2) del 78,45%; non contiene idrocarburi aromatici, ad esempio, le emissioni di idrocarburi aromatici ad anelli condensati (es: benzopireni) sono ridotti fino al 71%; non ha emissioni di diossido di zolfo (SO2), dato che non contiene zolfo; ha una minore infiammabilità; è biodegradabile nelle acque superficiali; non è tossico, anche se a contatto con la pelle produce una leggera irritazione; riduce i costi dello smaltimento degli oli esausti. Il biodiesel può essere impiegato nei motori diesel in miscele con il gasolio oppure puro, nonostante alcuni veicoli meno recenti possano subire una degradazione di tubi e giunti da parte del biodiesel che può intasare le vie di alimentazione del veicolo. Nei motori è usato come additivo al gasolio e migliora il potere lubrificante, inoltre aiuta a mantenere pulito il motore sciogliendo eventuali residui. In qualsiasi motore diesel moderno può essere usato puro, ma quando viene utilizzato a elevate concentrazioni bisogna fare alcune modifiche al motore per evitare problemi di prestazioni. Il biodiesel può essere anche impiegato per produrre energia elettrica e termica con costi più competitivi rispetto ad altri combustibili di origine fossile. Il suo impiego per il riscaldamento in caldaie è una pratica diffusa e testata, in cui è solitamente utilizzato puro al 100%.
Il lavoro sul riciclo degli oli vegetali esausti, ci ha spinto a intraprendere un percorso di estrazione di oli essenziali [6] da scarti vegetali e a pensare, sempre in un’ottica di economia circolare, di preparare prodotti per la cura della persona utilizzando sia gli oli essenziali che l’olio di oliva. Nel corso dell’anno scolastico 2022-23 è stato realizzato un progetto PTOF di ampliamento dell’offerta formativa, che ha coinvolto le classi del triennio della specializzazione chimica e materiali del nostro istituto. La finalità del progetto è stata quella di incrementare alcune delle competenze chiave europee come competenza personale, sociale e capacità di imparare a imparare, competenza sociale e civica in materia di cittadinanza e competenza imprenditoriale. Inoltre, il progetto ha consentito di far crescere negli alunni la consapevolezza di perseguire sempre più obiettivi tesi all’assunzione di responsabilità, nonché alla solidarietà, alla cura dei beni comuni e alla consapevolezza dei diritti e dei doveri. Ha reso anche possibile il potenziamento delle conoscenze in materia giuridica ed economico-finanziaria e di educazione all’autoimprenditorialità.

Figura 10. Strumentazione di laboratorio
Gli oli essenziali sono il prodotto del metabolismo secondario delle piante. La Farmacopea Europea 6.0 e le versioni successive riportano la seguente definizione: “Un olio essenziale è il prodotto della distillazione in corrente di vapore o dell’idro-distillazione, o della distillazione secca di una pianta o talune sue parti o, ancora, nel caso di prodotti agrumari, mediante opportuni processi meccanici a freddo”. La distillazione in corrente di vapore (Figura 10) è il metodo principalmente utilizzato per estrarre da una miscela alcune sostanze volatili termolabili.
Molte sostanze naturali aromatiche vengono estratte dalle piante con questo sistema: il vapore acqueo passa attraverso le fibre (in genere di cellulosa) contenenti la sostanza aromatica, che sotto forma di vapore va a mescolarsi col vapore acqueo. Dentro il condensatore entrambe le sostanze passano allo stato liquido e sono raccolte all’uscita del condensatore. La miscela di liquidi così formatasi viene separata tramite imbuto separatore.
Questa metodica si presta particolarmente per l’estrazione di essenze quali limonene, olio di lavanda, rosmarino, menta, salvia, alloro, cinnamaldeide (cannella) e altri. Gli oli essenziali sono composti da una miscela complessa di molecole estremamente volatili e fragranti di varia natura chimica, come idrocarburi mono- e sesquiterpenici e materiali ossigenati, fenil propanoidi derivati, composti del metabolismo di acidi grassi e amminoacidi, composti azotati e solforati (Figura 11); hanno un odore forte, gradevole, sono perlopiù incolori o leggermente colorati, sono molto solubili in alcol, grassi, acido acetico, etere, cloroformio e hanno peso specifico inferiore dell’acqua (Eccezioni: olio essenziale di Cannella, Garofano e Senape).
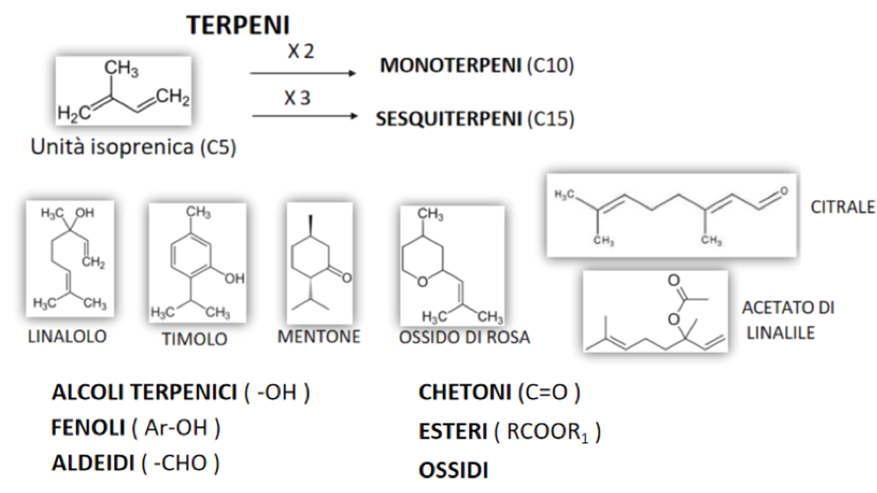
Figura 11. Alcuni componenti degli oli essenziali
Le principali proprietà fisiche degli oli essenziali sono odorosità, volatilità e oleosità. Per volatilità si intende la capacità dell’olio essenziale di evaporare e di diffondersi nell’aria a causa dell’elevata tensione di vapore; l’oleosità è, invece, la capacità di essere liposolubile, cioè di superare la barriera costituita dalle cellule epidermiche e venire facilmente assorbito attraverso la pelle. La caratteristica più significativa è l’odorosità, che consiste nella possibilità da parte del nostro olfatto di rilevare gli oli essenziali come odori. Le cellule olfattive, sollecitate dalle molecole odorose, trasformano lo stimolo chimico in impulsi elettrici che vanno ad attivare i centri nervosi (Figura 12).
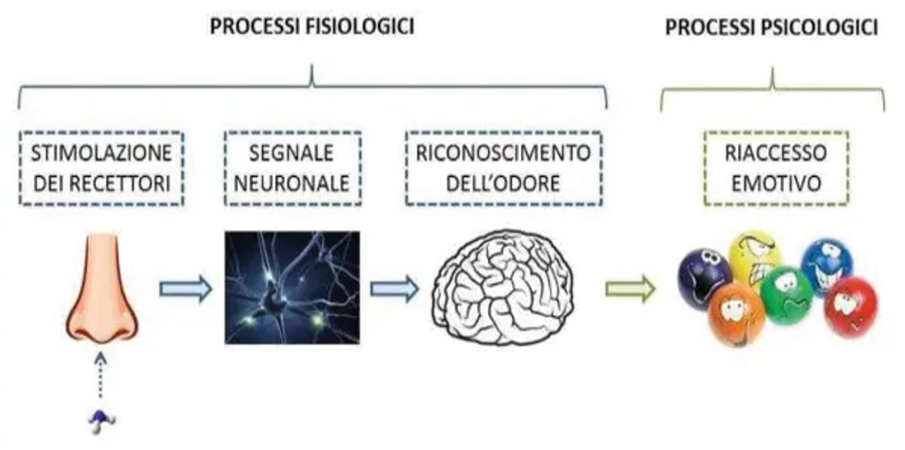
Figura 12. Fisiologia dell’olfatto (tratto da www.tecnosida.it)
In seguito, vengono esaminate alcune caratteristiche degli oli essenziali ottenuti durante l’attività laboratoriale. L’olio essenziale di lavanda, preparato mediante distillazione in corrente di vapore delle infiorescenze, contiene composti terpenici e trova impiego nell’aromaterapia, nella cosmetica e in campo farmaceutico. Può essere utilizzato come rimedio antifungino per acne, forfora, prurito da punture d’insetto e anche infezioni batteriche.
Nei laboratori didattici del nostro Istituto è stato ottenuto anche l’olio essenziale di arancia dolce mediante distillazione in corrente di vapore delle bucce, anziché con il metodo generalmente utilizzato della spremitura a freddo. L’olio di arancia ha numerose azioni benefiche per il corpo: antispasmodico, ha un’azione rilassante sulla muscolatura, è quindi indicato in caso tensione muscolare; sedativo, aiuta a combattere l’insonnia; levigante e ringiovanente, contrasta la formazione di rughe e smagliature.
La composizione dell’olio è stata verificata mediante analisi GC-MS. I composti principali sono: limonene, terpinene, citrale e altri in tracce.
Analogamente, l’olio essenziale di alloro ottenuto dalle foglie è stato caratterizzato mediante GC-MS evidenziando che i componenti principali sono eucaliptolo, linalolo, α-pinene, mircene ed eugenolo. Esso aiuta a contrastare influenza e raffreddore grazie alla sua azione battericida e balsamica; ha anche azione digestiva, carminativa ed è indicato in caso di dispepsia e gonfiore di stomaco. In aromaterapia è utile in caso di stanchezza, esaurimento e stress.
L’olio laurino è l’ingrediente peculiare dell’antichissimo sapone di Aleppo. Veniva inoltre utilizzato per preservare libri e pergamene e per preparare le classiche coroncine d’alloro. L’olio essenziale di cannella è stato ottenuto per distillazione in corrente di vapore dalla corteccia secca dell’albero. È un potente antisettico, stimolante della circolazione, riscaldante, antispasmodico, digestivo, carminativo, antinfiammatorio, tonico e stimolante generale, antiparassitario. L’analisi della composizione ha messo in evidenza la presenza di aldeide cinnamica, eugenolo e cariofillene.
5. Impiego degli oli essenziali
Nel corso dell’attività laboratoriale, una volta estratti gli oli sono stati utilizzati per produrre creme, saponi e candele profumate (Figura 13).
Per ottenere la crema, in una ciotola si uniscono l’olio di oliva, l’olio di mandorle dolci, la cera d’api e si mette a bagnomaria fino a dissoluzione della cera. Si fa raffreddare e si addiziona un poco alla volta, mescolando, il gel di aloe a cui era stata aggiunta la soluzione satura di acido citrico che funge da stabilizzante. Si frulla il tutto con frullatore a immersione per 20 minuti in modo da ottenere una consistenza morbida; alla fine si aggiunge l’olio essenziale, la vitamina E e si conserva in barattolo chiuso.
Per il sapone si scioglie l’idrossido di sodio nell’acqua e si riscalda fino a 40/45°C. Si aggiunge la soluzione all’olio di oliva e si frulla fino al raggiungimento del cosiddetto “nastro”, ovvero quando i grassi e la soluzione liquido/soda caustica si sono emulsionati in modo tale da permettere la corretta saponificazione del composto. Si aggiunge la profumazione e si lascia maturare nello stampo per 40 giorni.
Infine, le candele profumate si ottengono ponendo la cera in un becher a bagnomaria. Quando la cera è fusa viene amalgamata con una spatola e successivamente si aggiunge del colorante e qualche goccia di olio essenziale.

Figura 13. Prodotti realizzati in laboratorio
Le procedure sopradescritte sono state eseguite sia nei laboratori didattici che presso una struttura residenziale per anziani consentendo l’applicazione della metodologia del Service Learning. Con tale metodologia l’alunno mette in pratica ciò che viene appreso a scuola nel proprio contesto di vita per incentivare la costruzione di nuovi apprendimenti e puntare al bene comune. In questo modo lo studente acquisisce abilità e competenze in ambito tecnico-scientifico per inserirsi nel mondo del lavoro e delle professioni, ma se l’apprendimento è messo a servizio degli altri, serve anche a trarre ulteriori insegnamenti di tipo pro-sociale: “servire” insegna a essere persone complete che conoscono, ma sanno anche imprimere cambiamenti per migliorare la realtà. Il Service Learning coniuga lo sviluppo della mente, che impara a pensare, della mano, che imprime un cambiamento con il fare, e del cuore, che si rende disponibile verso gli altri. Come ha detto Edgar Morin [7]: “Meglio una testa ben fatta che una testa ben piena”, nel senso che una testa ben fatta dispone di un’attitudine a trattare i problemi e approfondirli, a collegare tra loro i saperi conferendo loro un senso. Il Service Learning è un approccio pedagogico grazie al quale gli studenti apprendono attraverso la partecipazione attiva. Esso unisce due aspetti fondamentali:
• Service, l’esperienza di servizio alla comunità, la cittadinanza e le azioni solidali;
• Learning, l’esperienza di apprendimento e di studio, l’acquisizione di capacità e competenza di diverso tipo (da quelle didattiche e metodologiche a quelle sociali).
Il Service Learning chiede agli studenti di compiere azioni solidali concrete nei confronti della comunità, creando così un circolo virtuoso tra apprendimento (learning) e servizio solidale (service). Non è un metodo con regole predefinite: l’elemento innovativo sta nell’imparare agendo attraverso un approccio metodologico capace, al tempo stesso, di potenziare i valori della cittadinanza attiva in modo da far interiorizzare agli studenti i valori dell’uguaglianza, della giustizia, della legalità, del rispetto per l’ambiente. La partecipazione da protagonisti degli studenti va dalla fase iniziale di pianificazione fino alla valutazione conclusiva.
Infatti, gli studenti, con i loro bisogni e i loro desideri, costituiscono il punto di partenza e di arrivo di ogni proposta didattica, includendo contenuti curricolari, riflessioni, sviluppo di competenze per la cittadinanza, mentre gli adulti (insegnanti, dirigenti scolastici, responsabili del territorio, genitori) devono limitarsi ad accompagnarli e sostenerli, restando nell’ombra. Gli studenti sperimentano così la fiducia nei propri confronti e diventano capaci di assumersi responsabilità, di migliorare la qualità di vita delle persone, prendendosi cura degli altri e dell’ambiente, creando un solido legame tra scuola e comunità sociale, in un’ottica inclusiva. Nello stesso tempo il Service Learning è un’esperienza di vita anche per i docenti stessi, i quali non si pongono davanti agli alunni, ma stanno al loro fianco, vivendo insieme l’esperienza che diventa concretamente competenza e accoglienza. Insomma, è un vero e proprio percorso di crescita, oltre che del singolo, della classe nel suo insieme.
Il lavoro svolto nella sua interezza ha costituito un percorso di approfondimento di conoscenze già in possesso degli allievi e di miglioramento delle competenze degli stessi, sia dal punto di vista professionale che personale.
[1] G. Rizzitano, Laboratorio ed Esercitazioni di chimica Agraria, Edagricole scolastico, 2002.
[2] Determinazione dell’acidità organica dell’olio, in G. Rizzitano, Laboratorio ed Esercitazioni di chimica Agraria, Edagricole scolastico, 2002, p. 287.
[3] Determinazione del numero di perossidi dell’olio, in G. Rizzitano, Laboratorio ed Esercitazioni di chimica Agraria, Edagricole scolastico, 2002, p. 289.
[4] Analisi spettrofotometrica dell’olio, in G. Rizzitano, Laboratorio ed Esercitazioni di chimica Agraria, Edagricole scolastico, 2002, p. 299.
[5] Determinazione del numero di saponificazione dell’olio, in G. Rizzitano, Laboratorio ed Esercitazioni di chimica Agraria, Edagricole scolastico, 2002, p. 294.
[6] E. J. Bowles, La chimica degli oli essenziali aromaterapici, Aracne, 2019.
[7] E. Morin, La testa ben fatta, Riforma dell’insegnamento e riforma del pensiero, Raffaelo Cortina, 1999.