La strumentazione scientifica e la cultura
Vedere le arie attraverso il bagno pneumatico
Eleonora Aquilini e Antonio Testoni
Divisione Didattica della Società Chimica Italiana (DD-SCI)
e-mail: ele.aquilini6@gmail.com; antonio.testoni55@gmail.com
Abstract. The gaseous state is, from an educational point of view, a difficult state of matter to deal with and acquire. Studying gases presents considerable cognitive difficulties because their materiality is not perceived. In fact, while the solid and liquid states have always been consciously perceived and used by mankind, the gaseous state only began to exist recently, at the beginning of the eighteenth century (Hales, Black), although phenomena and experiments involving gases had been known since antiquity. The study of gases was made possible thanks to the pneumatic bath. Understanding the importance of this instrument for the birth of chemistry as a science has great cultural and educational value.
Keywords: gas; bagno pneumatico; aria fissa; didattica; cultura
Con questo intervento ci proponiamo di illustrare l’importanza non solo nella storia della chimica, ma più in generale nella storia della scienza, di uno strumento antico - peraltro molto semplice nella sua costituzione e nella sua realizzazione - come il bagno pneumatico, sottolineando la sua valenza didattica e culturale che lo accomuna a tanti altri “strumenti antichi”. Se abbiamo a cuore la dimensione culturale della strumentazione scientifica e della stessa scienza non possiamo non affrontare questioni che riguardano le strategie e i processi di costruzione e di evoluzione della conoscenza.
Il “Come facciamo a sapere che…?”, il “Perché accettiamo o crediamo che…?”, “Quali sono le prove per…?”1dovrebbero essere parti irrinunciabili della nostra cultura, del nostro pensiero. Questioni che, calate in ambito scientifico, sono strettamente intrecciate con la strumentazione utilizzata. Sono, infatti, gli strumenti che permettono di conferire realtà alle più ingegnose congetture scientifiche2 e, nello stesso tempo, sono le teorie e le ipotesi che spesso ne guidano l’invenzione e il perfezionamento, facendo emergere il ruolo cognitivo che compete alla strumentazione scientifica, cioè quello di dispositivi indispensabili per la costruzione e la comprensione dei concetti scientifici. Di questo ne erano già ben consapevoli coloro che diedero il via alla rivoluzione scientifica (Francis Bacon, Novum Organum, 1620): “Non la sola mano, o l’intelletto in sé possono sussistere; tutto si compie mediante gli strumenti e i mezzi ausiliari”
È proprio con gli strumenti che, fra l’altro, possiamo vedere cose inimmaginabili alla percezione diretta. Gli esempi che di solito vengono fatti sono quelli del microscopio e del cannocchiale, raramente viene citato il bagno pneumatico, che è stato invece fondamentale per lo studio delle “invisibili arie”. A proposito di “arie” e di aria, già Boyle aveva rilevato che “La maggioranza della gente è talmente avvezza a giudicare le cose sul fondamento dei suoi sensi, che, a causa della invisibilità dell’aria, ad essa non assegnano alcun attributo e la considerano come un niente.”3
Una concezione che a distanza di circa 400 anni è ancora ben presente!
Ancora oggi lo stato gassoso presenta notevoli problemi cognitivi. Studi e ricerche fatte con bambini e adolescenti hanno evidenziato che alcune idee sono molto radicate e difficili da scalfire, in particolare la convinzione che i gas non abbiano peso (massa), ossia non siano costituiti di materia. Rispetto allo stato solido e allo stato liquido esiste la stessa asimmetria che si riscontra nella storia dell’uomo: mentre lo stato solido e liquido sono sempre stati percepiti e usati consapevolmente dall’umanità, lo stato gassoso ha iniziato a esistere solo recentemente, agli inizi del Settecento (Hales, Black), sebbene fenomeni ed esperimenti nei quali erano implicati gas fossero noti dall’antichità.
Le differenti identità degli aeriformi poterono essere individuate solo grazie a un approccio prettamente chimico e non prima che si realizzasse quel passaggio cruciale costituito dall’introduzione di strumenti atti a contenerli e manipolarli, sulla scia di quelli utilizzati da Torricelli e da Boyle. Infatti, le scoperte di Torricelli e di Boyle furono possibili grazie all’invenzione di particolari dispositivi che permettevano di “vedere” l’aria e di poterla osservare in modo talmente accurato da poterne misurare alcune proprietà. Per tutto il Settecento, il bagno pneumatico (Figura 1) divenne lo strumento fondamentale della chimica e assurse al ruolo di “microscopio” della chimica dopo che Hales iniziò a utilizzarlo in modo insolito per raccogliere le arie che si producevano in seguito a trasformazioni chimiche.
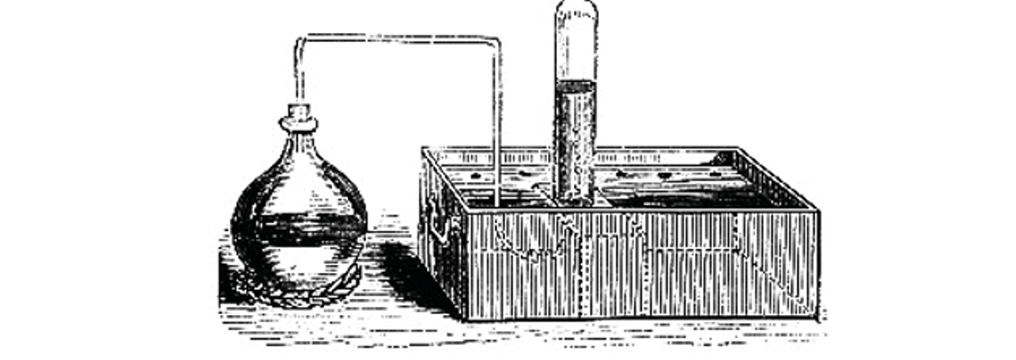
Figura 1. Bagno pneumatico
Utilizzato in questo modo, il bagno pneumatico permise nell’arco di 50 anni di popolare lo stato gassoso con “individui” diversi che inizialmente vennero chiamate “arie”. Il bagno pneumatico permise, da una parte, di scoprire il terzo stato di aggregazione della materia, quello gassoso e, dall’altra, di sviluppare la chimica delle arie. Diventò, cioè, possibile osservare in modo completamente nuovo innumerevoli trasformazioni chimiche, note da secoli o millenni quali, ad esempio, la calcinazione del calcare.
carbonato di calcio (+ calore) → calce
Fin dal 2500 a.C. i popoli della Mesopotamia avevano imparato a trasformare il calcare in calce, avevano infatti constatato che la pietra calcarea, con il riscaldamento ad alte temperature, si trasformava in un’altra sostanza, la calce, parzialmente solubile in acqua e con la proprietà fondamentale di comportarsi da legante (ancora oggi la calce si ottiene in questo modo). Era altresì noto, ai tempi di Hales, che la calce esposta all’aria si ritrasformava lentamente in calcare e che il calcare, a contatto con un acido come l’acido cloridrico, sviluppava un gas e formava un sale (cloruro di calcio), lo stesso sale che si otteneva facendo reagire la calce con l’acido medesimo senza alcun sviluppo di gas. Hales osò ipotizzare che il calcare fosse formato da calce e aria, la quale poteva essere liberata in seguito ad un riscaldamento energico. Il bagno pneumatico (Figura 2) fu decisivo per confermare quella che sembrava essere un’azzardata e “fantasiosa” ipotesi:
calcare (+ calore) → calce + aria
Soltanto per mezzo del bagno pneumatico:
• l’aria, liberatasi durante la calcinazione del calcare, diventava finalmente un fatto, un fenomeno osservabile
• diventava possibile, andando oltre le apparenze, conoscere la realtà

Figura 2. Bagno pneumatico di S. Hales
Le scoperte di Hales costituirono comunque l’atto di nascita del concetto di gas in quanto per la prima volta fu possibile confermare sperimentalmente che molte sostanze solide e liquide erano composte anche di aria, o detto in altri termini, che l’aria era chimicamente attiva (cioè l’aria partecipava a molte trasformazioni chimiche). Questa fu un’acquisizione scientifica fondamentale. Fin dall’antichità non era sfuggito il fatto che l’aria fosse essenziale in molte trasformazioni, ma ciò che per millenni non era stato compreso era la funzione chimica dell’aria.
Il passaggio successivo, altrettanto importante, lo si deve al chimico scozzese J. Black. Nel 1755, Black in seguito ai suoi studi sulla magnesia alba (carbonato basico di magnesio) verificò che anch’essa, una volta calcinata, produceva della calce (di magnesio) e dell’aria in modo del tutto simile al calcare. Però, a differenza di Hales, Black si pose il problema di verificare se quell’aria fosse effettivamente uguale all’aria comune e giunse alla conclusione che era diversa. Questo primo gas scoperto oltre l’aria atmosferica venne chiamato da Black aria fissa: egli voleva con ciò intendere che quel gas, diverso dall’aria atmosferica, era contenuto (fissato) nel calcare:
calcare (+ calore) →. calce + aria fissa
Le caratteristiche più significative di questo gas, che permisero a Black di differenziarlo dall’aria atmosferica, furono le seguenti:
- non manteneva la combustione;
- non permetteva la respirazione;
- formava rapidamente un precipitato con l’acqua di calce.
L’ipotesi dell’aria fissa costituì non solo un miglioramento dell’intuizione di Hales, ma ebbe una grande importanza perché:
• per la prima volta venne ipotizzata l’esistenza di un gas diverso dall’aria atmosferica
• permise finalmente di spiegare, oltre la calcinazione del calcare, una molteplicità di fenomeni noti da molto tempo (caustificazione della soda e della potassa, la diversa aggressività della soda e della soda caustica, …)
• aprì la strada alla ricerca e allo studio di nuove arie (Priestley, Cavendish, Scheele) che costituirono il terreno su cui si sviluppò la cosiddetta “chimica pneumatica”.4
Ma è con Lavoisier che le nuove arie e i fenomeni a esse collegati vennero finalmente inquadrati in un solido e convincente sistema teorico, come mai si era visto prima. Nelle mani di Lavoisier la bilancia e il bagno pneumatico (Figura 3) divennero gli strumenti fondamentali per attuare quella rivoluzione di pensiero e di metodo che trasformò la chimica in una “scienza esatta”. Anche per la chimica, come era già avvenuto nel secolo precedente per la fisica, il superamento della fase prescientifica si realizzò con l’individuazione di concetti quantitativi (in particolare il principio di conservazione della massa/peso). Questo fu possibile grazie all’uso di strumenti di misura e il bagno pneumatico, proprio con Lavoisier, divenne anche uno strumento di misura. Il ricorso sistematico a strumenti di misura fu un passaggio fondamentale perché è con la misura che si pone in relazione (biunivoca) il mondo degli oggetti reali e il mondo degli “oggetti immaginari” della matematica e questa è la prima fondamentale astrazione del ragionamento scientifico. Astrazione che è necessaria proprio per poter usare lo strumento matematico, senza il quale non sarebbe possibile alcuna articolazione, alcun linguaggio, alcuna legge scientifica. La matematizzazione della natura è il tratto distintivo delle scienze e anche per la chimica, pur nella sua specificità, la matematizzazione costituì il passaggio decisivo. Nacque la chimica di Lavoisier, una chimica moderna: la nostra chimica!
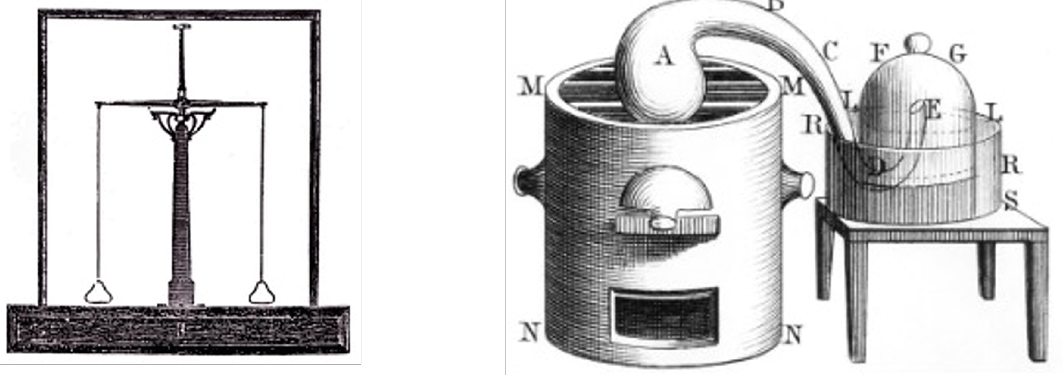
Figura 3. La bilancia e il bagno pneumatico: gli strumenti di misura di Lavoisier
Anche dopo Lavoisier il bagno pneumatico continuò a essere uno strumento (di misura) indispensabile. Con esso, ad esempio, Gay-Lussac ricavò la legge dei rapporti volumetrici delle reazioni in fase gassosa che venne poi interpretata da Avogadro alla luce della nascente teoria atomica (volumi uguali di gas diversi …). Proprio la legge di Avogadro, nelle mani di Cannizzaro, risultò decisiva per ricavare quei pesi atomici esatti senza i quali Mendeleev non avrebbe potuto inventare quella che è considerata l’icona della chimica, cioè la Tavola Periodica degli Elementi.
Ciò che, infine, vogliamo sottolineare è che “storie” come questa, con al centro strumenti scientifici del passato come il bagno pneumatico, vanno al cuore e colgono l’essenza stessa del pensiero scientifico, dove immaginazione, creatività e razionalità si incarnano nella materialità del mondo che ci circonda per conoscerlo ed interpretarlo.
È nostro compito tutelare e trasmettere alle generazioni future questo patrimonio di idee e di strumenti. Un patrimonio che è fondamentalmente culturale, perché, come ci ricorda e ci insegna questo grande filosofo e storico della scienza, quale è stato Paolo Rossi: “La razionalità, il rigore logico, la controllabilità delle asserzioni, la pubblicità dei risultati e dei metodi, la stessa struttura del sapere scientifico come qualcosa che è capace di crescere su se stesso, non sono categorie perenni dello spirito, ma conquiste storiche che, come tutte le conquiste, sono suscettibili di andare perdute”,5 se non ci impegniamo a preservarle e ad alimentarle continuamente.
1 A. B. Arons, Guida all’insegnamento della Fisica, Zanichelli, Bologna, 1992, pp. 366-368.
2 “Vivo in un paese barbaro dove i chimici sono così fraintesi e gli strumenti così difficili da procurarsi che è arduo elaborare delle ipotesi e sperimentarle” (R. Boyle) in Boyle, La chimica come scienza esatta, a cura di A. Gavezzotti, Grandangolo Scienza, RCS Mediagroup, 2016, pag. 21.
3 in “Ambigua, sfuggente... vitale” pubblicazione del Museo di Chimica, Università di Genova, 2006, pag. 1.
4 C. Fiorentini, A. Aquilini, E. Colombi, A. Testoni, Leggere il mondo oltre le apparenze, Armando, Roma, 2007.
5 P. Rossi, Il tempo dei maghi, Raffaello Cortina, Milano, 2006, pag. 304.