Abstract. Luigi Francesconi published several articles on the identification of the main components of Santolina chamaecyparissus L. essential oil. He identified three ketones into the essence, giving the structure of santolinenone α and β. These compounds do not exist, and the erroneous identification derives from a wrong interpretation of the experimental available data as well as from the fact that he did not carry out decisive experiments for the identification of the structure.
Keywords: Luigi Francesconi; olio essenziale della Santolina camaecyparissus; componenti dell’olio essenziale; la falsa identificazione del santolinenone α e β
Qualche tempo fa, leggendo un articolo su CnS ho conosciuto l’esperienza di una scuola di Acquapendente (Viterbo) che aveva prodotto l’olio essenziale della Santolina etrusca [1]. Prendo contatto con la scuola e mi offro di aiutarli a portare avanti il loro progetto, ammesso che potessi essere utile. Il mio aiuto si è concretizzato nell’analisi dell’olio essenziale utilizzando tecniche gascromatografiche [2].
Il componente principale dell’olio essenziale era il viridiflorolo, un sesquiterpene (Figura 1, sinistra), come si evince bene guardando il gascromatogramma dell’olio essenziale stesso (Figura 1, destra).
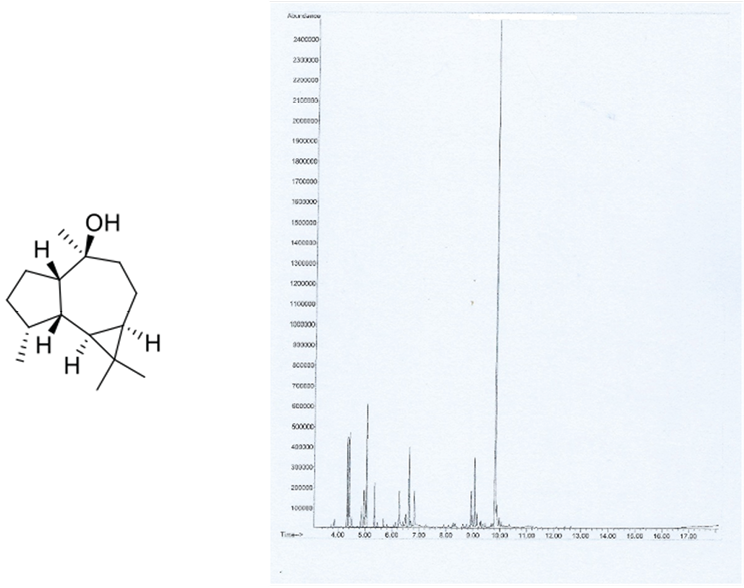
Figura 1. Struttura del viridiflorolo (destra) e gascromatogramma dell’olio essenziale di Santolina etrusca
Cerco di sapere qualche cosa di più su questa specie e le sue consimili e nella mia ricerca mi imbatto in un articolo molto datato, un articolo del 1911 scritto da Francesconi [3] sull’olio essenziale di una specie analoga, cioè Santolina chamaecyparissus L. (Figura 2).

Figura 2. Santolina chamaecyparissus
2. Luigi Francesconi e l’olio essenziale di Santolina chamaecyparissus
Nato a Tolentino nel 1864, Luigi Francesconi studia chimica a Roma, dove si laurea ed entra nel gruppo di Cannizzaro, nel quale si occupa insieme ad altri delle ricerche volte alla determinazione della struttura della santonina e dei suoi prodotti di degradazione. Ricerca di lunga durata, che, però, non si conclude con un successo: il gruppo non riuscirà a dare la struttura corretta della santonina che verrà chiarita solo dopo diversi anni [4, 5]. Nel 1905 Francesconi vince il concorso per la cattedra di chimica farmaceutica a Cagliari, dove inizia a dedicarsi allo studio delle essenze locali. Si occupa anche del rapporto fra struttura chimica e fluorescenza. Nel 1915 si trasferisce a Messina e nel 1917 a Genova, dove rimarrà per il resto della sua carriera fino al 1935. In questa sede si occuperà di radioattività naturale, del comportamento sotto irradiazione UV di acidi grassi e del comportamento chimico della vitamina D2. Divenuto professore emerito continua a occuparsi di ricerca scientifica in un laboratorio costruito nella sua abitazione fino alla morte avvenuta il 30 dicembre del 1939.
Proprio studiando le piante autoctone della Sardegna, Francesconi si imbatte nella Santolina camaecyparissus. Prima di affrontare quello che Francesconi scriverà sulla composizione dell’olio essenziale è bene cercare di definire cosa si conosce sulla composizione del suo olio essenziale. Quello che appare evidente è che si osserva una grande variabilità della composizione in funzione del luogo in cui la pianta è stata raccolta (Tabella 1) [6-13]. In tutti i casi i componenti principali sono mono- e sesquiterpeni (Figura 3).
Tabella 1. Componenti principali identificati nell’olio di Santolina chamaecyparissus in luoghi differenti
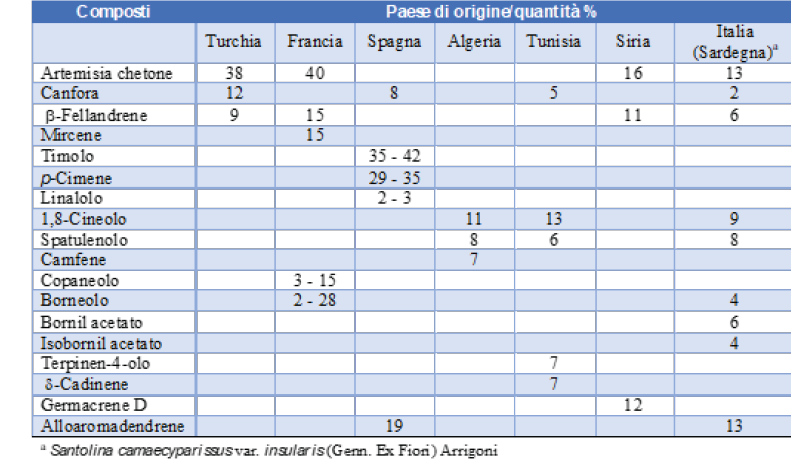

Figura 3. Monoterpeni e sesquiterpeni trovati come componenti principali nell’olio essenziale di Santolina chamaecyparissus
A questo punto, sapendo cosa cercare, vediamo quello che a suo tempo scrisse Francesconi. Nell’articolo sopra citato [3], viene descritta la procedura per ottenere l’olio essenziale (una distillazione in corrente di vapore) e il frazionamento dell’olio essenziale così ottenuto per distillazione in corrente di vapore. Le frazioni ottenute per distillazione sono state sottoposte ad analisi elementare ottenendo risultati come quelli mostrati nella Tabella 2.
Tabella 2. Analisi elementare delle frazioni di distillazione
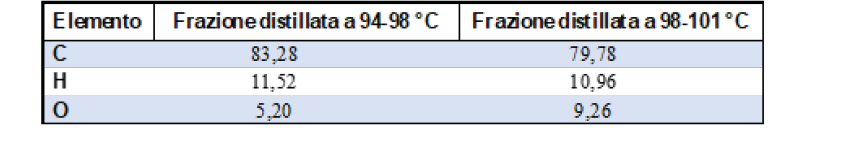
Francesconi non riesce a isolare sostanze pure, tuttavia le analisi sembrano essere in accordo con una composizione in cui prevalgono specie con formula bruta C10H16O. Il numero di atomi di carbonio fa pensare a monoterpeni contenenti ossigeno.
Francesconi non si ferma qui. Negli anni successivi continuerà a occuparsi del problema cercando di risolvere la questione dell’identificazione del componente principale presente nell’olio essenziale. Le frazioni distillate non contengono le funzioni alcolica, fenolica e acida. La presenza dell’ossigeno sembra legata alla presenza di un gruppo carbonilico. Il gruppo carbonilico appartiene a un chetone dato per il quale non si ha reazione nei saggi relativi alla presenza di aldeidi. Non riuscendo a isolare una sostanza pura, Francesconi tratta il gruppo carbonilico con idrossilammina in ambiente basico così da ottenere la corrispondente ossima. Da questa reazione in un primo momento isola la idrossilamminossima di un chetone (ossima del chetone dove l’idrossilammina ha dato anche un’addizione coniugata al doppio legame), l’ossima dello stesso chetone, l’ossima di un altro chetone e un’idrossilammina derivante dal secondo chetone. Questi dati gli fanno ritenere che il composto contenga un solo doppio legame [14].
Da queste informazioni Francesconi deduce che [15]:
- Nell’essenza … è contenuto un composto carbonilico, probabilmente un chetone con formula C10H16O
- Detto chetone ha almeno un doppio legame e quindi è a catena aperta con due doppi legami, o a catena chiusa, monociclico non saturo con un solo doppio legame
- Il doppio legame sta fra due atomi di carbonio in posizione βγ rispetto al carbonile (α)
Dato che si ottiene un solo prodotto di addizione dell’idrossilammina a un doppio legame, Francesconi si convince che nella molecola c’è solo un doppio legame. Dal comportamento chimico dell’idrossilamminossima deriva che la struttura del chetone deve contenere la sequenza strutturale descritta nella figura 4.
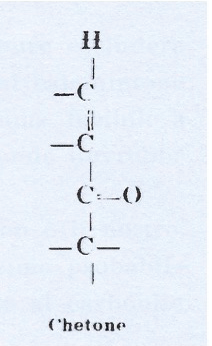
Figura 4. Sequenza strutturale identificata da Francesconi
Questa sequenza, sapendo cosa può contenere l’olio essenziale, fa pensare immediatamente all’artemisia chetone. Francesconi, invece, non considerando possibile la presenza di un altro doppio legame non coniugato, opta per una struttura ciclica e propone [16] la struttura del santolinenone α (Figura 5).
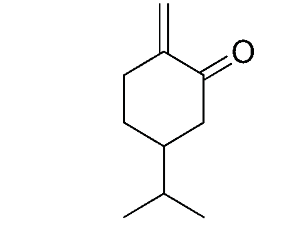
Figura 5. Santolinenone α
Continuando lo studio dei componenti dell’olio essenziale Francesconi trova un terzo chetone, sempre con formula C10H16O, che non sembra essere correlato al santolinenone, ma alla canfora [16]. Oggi è noto che la canfora può essere presente nell’olio essenziale.
Se la miscela delle ossime viene trattata con acidi si ottiene il chetone di partenza la cui analisi elementare è in accordo con la formula C10H16O [17]. Inoltre, prendendo in considerazione la idrossilamminossima del santolinenone α, sulla base della struttura assegnata questa contiene due atomi di carbonio asimmetrici (Figura 6).
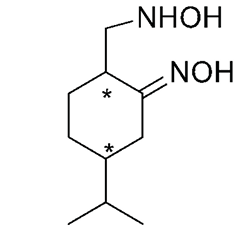
Figura 6. Atomi di carbonio asimmetrico nell’idrossilamminossima del santolinenone α
Anche l’ossima del santolinenone α ha un atomo di carbonio asimmetrico e dovrebbe essere risolvibile nei suoi enantiomeri. Francesconi, però, inspiegabilmente, tenta la risoluzione con acido canforsolfonico chirale della sola idrossilaminossima, riuscendo a separare un sale con attività ottica [18].
L’ultimo passo da parte Francesconi è quello di assegnare una struttura al santolinenone β. Sulla base in gran parte della considerazione che questo composto, se trattato con idrossilammina, non dà l’idrossilamminossima ma solo un derivato idrossilamminico e l’ossima, vengono proposte [19] due possibili strutture (Figura 7).

Figura 7. Strutture proposte per il santolinenone β
Questi risultati non collimano per nulla con quello che oggi è noto sulla composizione dell’olio essenziale della Santolina chamaecyparissus. Già nel 1964, un lavoro statunitense ha messo in dubbio le formule proposte da Francesconi e rianalizzando l’olio essenziale ha identificato solo l’artemisia chetone [20].
È possibile, quindi, che Francesconi abbia sottovalutato la possibilità che nell’olio essenziale ci fosse un composto a catena aperta contenente due doppi legami per sposare la tesi del composto ciclico. A questo punto le due ossime che Francesconi osserva dovrebbero essere gli isomeri sin e anti delle ossime dello stesso composto, l’artemisia chetone. L’artemisia chetone, per dare una possibile giustificazione al suo operato, non era noto all’epoca di Francesconi. La struttura del 3,3,6-trimetilepta-1,5-dien-4-one, isolato da Artemisia annua L., inusuale per la sua struttura che presenta una giunzione isoprenica irregolare, è stata proposta solo nel 1920, dando, peraltro, una struttura sbagliata dato che è priva di un doppio legame coniugato [21], mentre la struttura corretta è stata stabilita nel 1964 in un articolo già citato [20].
Quella che qui si avanza è anch’essa solo un’ipotesi. Di fatti, un mio tentativo di capire se le ossime dell’artemisia chetone fossero state preparate e isolate ha dato un esito quasi fallimentare. In un solo articolo ho trovato la preparazione dell’ossima e questa è risultata un solido basso fondente di cui non veniva riportata l’isomeria geometrica delle ossime [22].
Si possono trarre delle conclusioni da quanto detto? Francesconi è arrivato a un passo dal determinare la struttura corretta del componente principale dell’olio essenziale di Santolina chamaecyparissus. Se non si fosse basato solo sul comportamento chimico verso il cloridrato di idrossilammina dell’estratto, ma avesse fatto qualche esperimento aggiuntivo (per esempio un’idrogenazione) avrebbe capito che la molecola con cui aveva a che fare ha due doppi legami e, quindi, deve essere a catena aperta. L’errore fa parte dell’esperienza del ricercatore; solo una grande prudenza nell’asseverazione dei risultati ci può proteggere dal commettere errori. Ma chi non li ha fatti?
Feyerabend, nel suo Contro il metodo, nota che i disegni della superficie lunare fatti da Galileo erano sbagliati e che, probabilmente, derivavano più dalle aberrazioni delle lenti del suo cannocchiale primordiale che da un’osservazione non corretta [23].
Di Trocchio ha ampiamente dimostrato come l’errore ha accompagnato gran parte delle scoperte scientifiche [24]. Tutti i chimici organici, qualche anno fa, rimasero colpiti dalla pubblicazione di un articolo su Angewandte Chemie dove una reazione veniva realizzata in maniera stereoselettiva se eseguita in presenza di un forte campo magnetico [25]. Anche questi risultati risultarono poi completamente falsi [26].
Tutti possono sbagliare, la scienza ha, però, un antidoto all’errore: gli esperimenti possono essere rifatti e questo può portare a scoprire l’errore e a correggerlo. Questo è il grande vantaggio del fare scienza.
[1] A. Adami, et al., “Le essenze della Tuscia” ovvero estrazione, analisi e attività antibatterica dell’olio essenziale di Santolina etrusca, CnS, 2019, 1, 21- 52.
[2] M. D’Auria, et al., Composition and seasonal variation of volatile organic compounds in Santolina etrusca (Lacaita) Marchi & D’Amato found at Acquapendente (Viterbo, Central Italy), Nat. Prod. Res., 2023, 37, 3310-3313.
[3] L. Francesconi, P. Scarafia, L’essenza della Santolina Chamaecyparissus L., Gazz. Chim. Ital., 1911, 41(II), 185-203.
[4] M. D’Auria, Alle origini della fotochimica in Italia. Cannizzaro e l’isomerizzazione fotochimica della santonina, Rendiconti della Accademia Nazionale delle Scienze detta dei XL, Memorie di Scienze Fisiche e Naturali, Serie V, 2015, 39, Parte II, Tomo II, 199-206.
[5] M. D’Auria, La lunga storia della santonina gialla, La Chimica e l’Industria Newsletter, 2017, 4(7), 17-23.
[6] M. J. Pérez-Alonso, A. Velasco-Negueruela, Essential oil components of Santolina chamaecyparissus L., Flav. Fragr. J., 1992, 7, 37-41.
[7] G. Grosso, et al., Supercritical fluid extraction of the volatile oil from Santolina chamaecyparissus, J. Sep. Sci., 2009, 32, 3215-3222.
[8] L. Zaiter, et al., Essential oil of Santolina africana Jord. & Fourr. and Santolina chamaecyparissus L., J. Essent. Oil Bearing Plants, 2015, 18, 1338-1342.
[9] K. B. H. Salah-Fatnassi, et al., Chemical composition, antibacterial and antifungal activities of flowerhead and root essential oils of Santolina chamaecyparissus L., growing wild in Tunisia, Saudi J. Biol. Sci., 2017, 24, 875-882.
[10] B. Demirci, T. Özek, K. H. C. Baser, Chemical composition of Santolina chamaecyparissus L. essential oil, J. Essent. Oil Res., 2000, 12, 625-627.
[11] M. Derbesy, J. Touche, A. Zola, The essential oil of Santolina chamaecyparissus L., J. Essent. Oil Res., 1989, 1, 269-275.
[12] M. J. Khubeiz, G. Mansoui, In vitro antifungal, antimicrobial properties and chemical composition of Santolina chamaecyparissus essential oil in Syria, Int. J. Toxicol. Pharmacol. Res., 2016, 8, 372-378.
[13] F. Poli, et al., Comparison between the essential oils of Santolina insularis (Genn. ex Fiori) Arrigoni and Santolina corsica Jord. Et Fourr. from the island of Sardinia (Italy), J. Ethnopharmacol., 1997, 56, 201-208.
[14] L. Francesconi, P. Scarafia, Essenza della Santolina Chamaecyparissus (azione dell’idrossilammina), Gazz. Chim. Ital., 1912, 42(I), 297-304.
[15] L. Francesconi, P. Scarafia, Essenza della Santolina Chamaecyparissus. Formula del Santolinen-one C10H16O, Gazz. Chim. Ital., 1913, 43(I), 90-95.
[16] L. Francesconi, N. Granata, La formula del Santolinenone α, Gazz. Chim. Ital., 1915, 45(I), 167-181.
[17] L. Francesconi, N. Granata, I componenti della essenza di santolina CH, Gazz. Chim. Ital., 1914, 44(II), 150-162.
[18] L. Francesconi, N. Granata, A. Sanna, α-Santolinenone. Formula e inattività ottica. Scissione del composto idrossilamminossimico, Gazz. Chim. Ital., 1914, 44(II), 354-366.
[19] L. Francesconi, N. Granata, La formula del santolinenone β, Gazz. Chim. Ital., 1916, 46(II), 251-256.
[20] L. H. Zalkov, D. R. Brannon, J. W. Uecke, On the occurrence of the Santolinenones, J. Org. Chem., 1964, 29, 2786-2787.
[21] W. A. Jacobs, R. C. Elderfield, The terpenes, saponins, and closely related compounds, Ann. Rev. Biochem., 1938, 7, 449-472.
[22] G. A. Atazhanova, et al., Synthesis and crystal structure of a pyrazole derivative of artemisia ketone, Chem. Nat. Compd., 2000, 36, 152-155.
[23] P. K. Feyerabend, Contro il metodo, Feltrinelli, Milano, 1979, pp. 101-115.
[24] F. Di Trocchio, Le bugie della scienza, Mondadori, Milano, 1993.
[25] G. Zadel, et al., Enantioselective reactions in a static magnetic field, Angew. Chem. Int. Ed., 1994, 33, 454-456.
[26] P. Gölitz, Enantioselective reactions in a static magnetic field - A false alarm!, Angew. Chem. Int. Ed., 1994, 33, 1457.