Abstract. The transition from common sense concepts to scientific concepts in school requires careful consideration of what and how to teach at different levels. Language must accompany the evolution of scientific concepts, so that the scientific language is not perceived as abstract and incomprehensible words. In chemistry, the word “acid” is often taken as an example of this conceptual transformation.
Keywords: concetti scientifici; acidi; linguaggio
Affrontando il problema del linguaggio vorrei iniziare da una definizione semplice, data da alunni di una scuola molto particolare, quella di Barbiana [1]:
La lingua poi è formata dai vocaboli d’ogni materia. Per cui bisogna sfiorare tutte le materie un po’ alla meglio per arricchirsi la parola. Essere dilettanti in tutto e specialisti solo nell’arte del parlare.
Questa osservazione traduce in realtà in maniera ottimale la trasversalità del linguaggio rispetto alle varie discipline, soprattutto nella scuola di base, dove le discipline non devono istruire degli specialisti, ma devono solo formare gli individui per essere cittadini capaci di capire e farsi capire. Del resto, anche Gramsci, come ci ricorda De Mauro, aveva sottolineato la connessione tra linguaggio e formazione [2]:
Gramsci [...] non dimentica mai d’insegnarci che è il linguaggio, quale luogo di conoscenza, espressone, interazione, è il linguaggio, il terreno su cui da alcune decine di millenni si gioca la grande partita che degli umani fa, quando la vincano, esseri pienamente capaci di senso e di storia. Ed è l’educazione, è la scuola lo spazio in cui nelle società anche appena sviluppate, singoli e ceti possono farsi classe e vincere quella diuturna partita sibi et alienis. Questo, penso, leggeva e ha spinto a leggere in Gramsci don Milani.
Ma restiamo a Gramsci; le sue osservazioni, infatti, ci tornano utili per definire uno dei termini dell’argomento che dobbiamo affrontare, quello di ‘senso comune’ [3]:
Ogni strato sociale ha il suo ‘senso comune’ e il suo ‘buon senso’, che sono in fondo la concezione della vita e dell’uomo più diffusa. Ogni corrente filosofica lascia una sedimentazione di ‘senso comune’: è questo il documento della sua effettualità storica. Il senso comune non è qualcosa d’irrigidito e d’immobile, ma si trasforma continuamente, arricchendosi di nozioni scientifiche e di opinioni filosofiche entrate nel costume. Il ‘senso comune è il folclore della filosofia e sta sempre di mezzo tra il folclore vero e proprio (cioè comunemente inteso) e la filosofia, la scienza e l’economia degli scienziati.
2. Il passaggio dai concetti di senso comune ai concetti scientifici
A scuola il passaggio dai concetti di senso comune ai concetti scientifici è, parafrasando Koyré, un passaggio dal mondo del pressappoco all’universo della precisione. Ci vuole lentezza nel modo di insegnare per promuovere la crescita dei concetti insieme al linguaggio. Ci sembra illuminante quanto scrive lo stesso Koyré a proposito dell’alchimia, chiedendosi se all’uomo del Medioevo e del Rinascimento mancassero solo gli strumenti di misura e il linguaggio per appartenere al mondo della precisione [4]:
Ci si può domandare tuttavia se questa doppia carenza non si spieghi proprio con la mentalità caratteristica, con la struttura del “mondo del pressappoco”. Ora, a questo riguardo, mi sembra che il caso dell’alchimia ci fornisca la risposta decisiva. In effetti nel corso della sua esistenza millenaria, essa, sola fra le scienze delle cose terrestri, è riuscita a costruirsi un vocabolario, una notazione e anche un’attrezzatura, di cui la nostra chimica ha conservato l’eredità. Essa ha accumulato tesori di osservazioni, ha compiuto migliaia di esperienze, ha anche fatto scoperte importanti. E tuttavia non è mai riuscita a fare un’esperienza precisa: questo perché non l’ha mai tentata. Le descrizioni delle operazioni alchimistiche non hanno niente in comune con le formule dei nostri laboratori: sono ricette di cucina, imprecise, approssimative, qualitative come quelle. E non è l’impossibilità materiale di eseguire le misure che arresta l’alchimista, egli non se ne serve, anche quando le abbia a portata di mano. Non gli manca il termometro, ma l’idea che il calore sia suscettibile di misura esatta. Così egli si accontenta dei termini di senso comune: fuoco vivo, fuoco lento, ecc., e non si serve quasi mai della bilancia. Eppure la bilancia esiste; anzi essa -quella degli orafi e dei gioiellieri- è relativamente precisa. È appunto questa la ragione per cui l’alchimista non ne fa uso. Se egli la usasse, sarebbe un chimico. Anzi, perché egli avesse idea di farne uso, bisognerebbe che già lo fosse.
Passare da una conoscenza di senso comune che è approssimativa, che non conta e non misura, a una conoscenza scientifica, che dà un peso ai fenomeni sia dal punto di vista qualitativo che quantitativo, è un’operazione che comporta un’organizzazione del curricolo diversa da quella usuale, basata solo sulle sequenze disciplinari stabilite dall’università.
Nel primo ciclo è indispensabile soffermarsi prevalentemente sugli aspetti qualitativi dei fenomeni, mentre nel secondo ciclo è importante privilegiare gli aspetti quantitativi collegati spesso a leggi e teorie della chimica.
È fondamentale conoscere i fenomeni, farsene una rappresentazione mentale, descriverli e interpretarli usando parole. Le parole devono essere semplici e appropriate ed esprimere dei concetti.
A tal proposito, pensiamo che la metodologia delle cinque fasi [5] sia particolarmente significativa, nell’ambito dell’insegnamento scientifico per la scuola di base, anche perché elimina il meccanismo perverso della “penalità” che segue allo sbaglio, perché fa sì che il lavoro nella scuola di base si sviluppi tramite definizioni operative che si costruiscono grazie al contributo di tutti gli alunni.
Vediamo nel dettaglio la metodologia proposta. Si parte con l’esperimento al quale segue la riflessione sull’esperienza (su quali contenuti e sul tipo di esperimento si dirà meglio nella sezione tre). Si descrive, si individuano somiglianze e differenze, si inizia a stabilire quella rete di connessioni che permetterà poi di giungere alla consapevolezza delle relazioni che caratterizzano un fenomeno. È fondamentale, in questa fase, che si scriva per mettere ordine nei pensieri, per passare da percezioni e considerazioni soggettive ad un primo tentativo di oggettivazione; non importa che si scriva bene dal punto di vista formale. Le considerazioni in questi scritti sono molto vicine al senso comune, le espressioni sono spesso dialettali e “familiari”, ma l’importante è che si colgano gli aspetti significativi del fenomeno descritto. Si mette ordine anche individuando le sequenze temporali dell’evento che si sta studiando. Segue poi la fase della discussione collettiva. Questo è il momento del confronto fra pari e con l’insegnante, che fa anche in modo di indirizzare la discussione verso un’elaborazione significativa delle osservazioni fatte. Ognuno qui confronta le proprie convinzioni, il suo modo di vedere, riconsidera e rielabora tenendo conto del parere degli altri. È importante sottolineare che tutte le idee hanno uguale diritto di cittadinanza, tutte possono essere messe in discussione da tutti. Nella discussione collettiva vince la ragionevolezza, la condivisione, il convincimento dopo prove ricorrenti.
La quarta fase è quella dell’affinamento della conoscenza che si traduce nella revisione della parte scritta: si corregge e si rivedono le proprie posizioni riscrivendo le frasi in modo aderente alle nuove acquisizioni. Non si parla di errori, ma di interpretazioni diverse che sono oggetto di nuovi ripensamenti e di nuove rielaborazioni per tutti.
La quinta fase è stata introdotta perché non tutti i bambini riescono a fare una sintesi scritta chiara dal punto di vista del contenuto con un linguaggio corretto. Allora l’insegnante, alla fine dell’attività che porta a una conclusione condivisa, utilizzando tutto il materiale prodotto, fa una sintesi scritta che gli alunni trascrivono sul quaderno; in questo modo tutti i bambini hanno la definizione, conquistata in modo operativo, in una forma linguisticamente corretta.
La metodologia delle cinque fasi è un modo per raccontare ciò che si sta studiando e la narrazione è necessaria per fare significato in ambito scientifico. Le modalità di costruzione delle storie sono però diverse a seconda che ci si riferisca al ciclo primario o alla scuola secondaria di secondo grado. Nella scuola di base si creano percorsi didattici in cui fenomenologie non troppo complicate dal punto di vista teorico vengono analizzate partendo da esperimenti sui quali è possibile discutere, fare ipotesi e ottenere conferme, giungendo a definizioni operative che sono la sintesi ovvero la conclusione a cui si è pervenuti. La definizione operativa è il frutto di più operazioni: si lavora manualmente sulle cose, si sviluppano ipotesi individuali e si confrontano con quelle degli altri, si esercita il pensiero logico, si elabora il linguaggio. Il risultato è costituito da una o più frasi linguisticamente corrette che riassumono il percorso didattico. Il procedimento è prevalentemente induttivo e porta a generalizzazioni che sono il frutto di astrazioni adeguate all’età degli alunni. La didattica laboratoriale per le scienze della scuola di base si concretizza quindi nella costruzione di definizioni operative.
Il modello metodologico-relazionale proposto si rifà ai quattro grandi della psicologia dell’educazione del ventesimo secolo: Dewey, Piaget, Vygotskij e Bruner. Per quanto concerne il ruolo del linguaggio nell’apprendimento ci sembra importante rilevare la grande importanza del contributo vygotskiano e, in particolare, del linguaggio scritto nello sviluppo della presa di coscienza, nell’acquisizione della conoscenza, nello sviluppo del pensiero.
Possiamo imparare, con questa modalità, argomenti che riguardano i passaggi di stato, le soluzioni, acidi, basi e sali, parole e concetti importanti per la chimica.
Quando successivamente si passa allo studio di leggi e teorie, allora le definizioni operative non sono più sufficienti a creare storie che tengano conto dei risultati a cui si è giunti in una determinata disciplina scientifica. Allora è necessaria una contestualizzazione storica ed epistemologica che ricostruisca gli ambiti teorici ed epistemologici in cui si è pervenuti ad una determinata convinzione scientifica. Si usa la storia della scienza per evidenziare i tratti cruciali, i nodi epistemologici che hanno portato all’elaborazione di una nuova teoria. In questo caso la generalizzazione è un concetto astratto lontano dal senso comune. Il procedimento logico non è induttivo. Fare percorsi didattici nei due ambiti di scuola è completamente diverso. Nonostante ciò, il legame fra i diversi tipi di storie ci deve essere.
3. Il caso degli acidi nel curricolo verticale nella scuola secondaria di primo e secondo grado
Nel primo ciclo è fondamentale lavorare sul concetto di trasformazione attraverso lo studio di fenomenologie comprensibili. Le trasformazioni definite a scopo didattico, come fisiche e chimiche, sono una componente essenziale delle conoscenze di base della chimica. Ci sembra significativo esemplificare con lo sviluppo del concetto di acido, come sia possibile costruire l’idea di trasformazione in chimica [6]. Le trasformazioni chimiche permettono di ottenere sostanze diverse dai reagenti. In altre parole, l’acqua “scioglie” il sale da cucina, si ottiene una soluzione e da questa si può riottenere, per evaporazione, il sale stesso. L’acido cloridrico “scioglie” il carbonato di calcio, insolubile in acqua, ma la sostanza che si ottiene, per evaporazione, non è più carbonato di calcio. Lo si capisce perché questa nuova sostanza è solubile in acqua. Ci si chiede allora se gli acidi “sciolgono” tutte le sostanze insolubili in acqua. Dalle diverse prove che vengono fatte con varie sostanze, come metalli e altri sali, si comprende che non è così. Il rame, ad esempio, non viene solubilizzato dall’acido cloridrico e invece forma una soluzione con l’acido nitrico. Questo punto viene approfondito nel biennio della scuola secondaria di secondo grado, come si illustrerà di seguito. La classe delle sostanze basiche e quella dei sali vengono poi trattate con lo stesso approccio. Questo percorso operativo sul concetto di acido, che è incentrato sull’acquisizione del concetto di trasformazione in chimica, comporta una trasformazione del linguaggio: la parola di senso comune “sciogliere” diventa “solubilizzare” e viene distinta da “fondere”; si acquisiscono operativamente parole come soluzione, soluto, solvente e poi miscuglio eterogeneo ed omogeneo. I concetti si definiscono insieme al linguaggio.
Nel biennio, dopo avere compreso il significato della gerarchia composizionale di Lavoisier (Figura 1), in cui i metalli si trasformano in ossidi (calci metalliche) quando reagiscono con l’ossigeno e i non metalli (i combustibili) diventano acidi reagendo sempre con l’ossigeno, si può affrontare il problema dell’acido nitrico che reagisce con il rame [7].

Figura 1. La gerarchia composizionale di Lavoisier
L’esperimento e la spiegazione che fornisce Lavoisier è un’interpretazione congruente con la sua teoria che ha un grande valore didattico.
Consideriamo la reazione:
rame + acido nitrico →soluzione azzurra + vapori rossi
Se viene realizzata raccogliendo i vapori in un bagno pneumatico (Figura 2), questi vapori non sono rossi, ma incolori. Non si ha nessuna modifica dell’indicatore (ad esempio, rosso metile) aggiunto nell’acqua del bagno pneumatico.

Figura 2. La raccolta in bagno pneumatico dei vapori derivanti
dalla reazione tra rame e acido nitrico
In base alla sua teoria sulla composizione dell’aria, Lavoisier riteneva che l’ossigeno si combinasse con i vapori incolori per dare poi vapori rossi. Questa ipotesi può essere verificata facendo reagire il gas incolore raccolto con il bagno pneumatico con l’ossigeno, ottenuto ad esempio per decomposizione dell’acqua ossigenata con diossido di manganese (Figura 3).

Figura 3. Il dispositivo necessario alla generazione di ossigeno dalla
reazione di diossido di manganese e acqua ossigenata (a destra nella foto)
Collegando il tubo di gomma sotto il cilindro contenente il gas incolore, si osserva che esso combinandosi con l’ossigeno, diventa bruno (Figura 4). Pian piano i vapori rossi scompaiono e aumenta l’acidità del liquido, acidità evidenziata dal cambio di colore dell’indicatore. Lavoisier confermò la presenza di acido nitrico nell’acqua, neutralizzando la soluzione con idrossido di sodio e verificando che il sale ottenuto era nitrato di sodio.

Figura 4. La reazione tra il gas incolore e l’ossigeno, con la comparsa del colore bruno
Si può schematizzare così la reazione, secondo l’interpretazione di Lavoisier: il rame “prende” l’ossigeno dall’acido nitrico, diventando ossido di rame. L’acido nitrico riacquista l’ossigeno che ha perduto dall’aria diventando aria nitrosa. In acqua l’aria nitrosa diventa l’acido nitrico che reagisce con l’ossido di rame, diventando nitrato di rame (Figura 5).
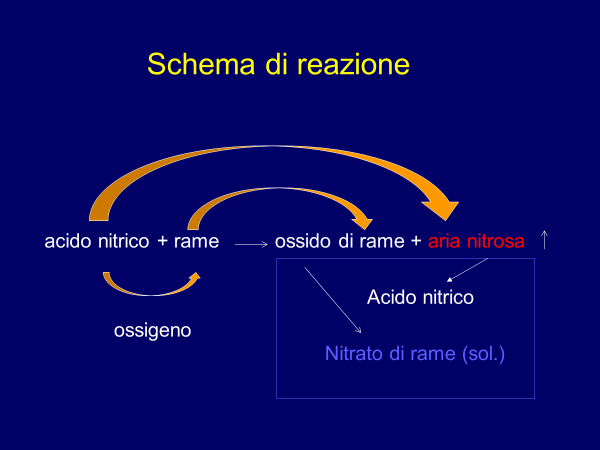
Figura 5. Lo schema di reazione complessivo secondo Lavoisier
Scaldando la soluzione azzurra si ottiene il sale, il nitrato si rame verde. Continuando il riscaldamento e collegando la beuta con un bagno pneumatico si ottiene una polvere nera (ossido di rame) e vapori rossi.
La reazione di discioglimento del rame con l’acido nitrico è un esempio di coerenza interpretativa dei dati sperimentali sulla base di una teoria. Il meccanismo di reazione che viene proposto è alla portata degli alunni del biennio e introduce al concetto di ossido-riduzione in modo operativo e non come conseguenza di reazioni a cui dei numeri, percepiti come magici, aumentano e diminuiscono senza ragione.
Il senso di lavorare secondo uno sviluppo verticale del curricolo è, dal mio punto di vista, costruire concetti importanti per la disciplina di interesse, nel nostro caso la chimica, avendo come punto focale la capacità di comprendere gli argomenti trattati da parte degli studenti. Il cammino viene tracciato avendo come guida lo sviluppo storico dei concetti stessi e la loro evoluzione. I concetti crescono insieme al linguaggio che è così ricco di contenuti. Nel passaggio dai concetti di senso comune a quelli scientifici le parole diventano sempre più astratte, ma il loro significato è rintracciabile nelle teorie di riferimento che sono una miniera di tesori che riflettono nelle parole il loro segreto splendore.
[1] Scuola di Barbiana, Lettera a una professoressa, Libreria Editrice Fiorentina, Firenze, 1969.
[2] T. De Mauro, Prima persona singolare passato prossimo indicativo, Bulzoni, Roma, 1998, p. 158.
[3] A. Gramsci, Quaderni del carcere, Einaudi, Torino, 1977, p. 2271.
[4] A. Koyré, Dal mondo del pressappoco all’universo della precisione, Einaudi, Torino, 1999, pp. 98 - 99
[5] C. Fiorentini, Il ruolo del laboratorio nell’insegnamento scientifico. 2 Una proposta metodologica per il primo ciclo di istruzione, Scuola e Didattica, 2005, n. 11, pp. 31 - 40.
[6] C. Fiorentini, Rinnovare l’insegnamento delle scienze, Aracne, Roma, 2018, pp. 302-304.
[7] C. Fiorentini, E. Aquilini, A. Testoni, D. Colombi, Leggere il mondo oltre le apparenze, Armando, Roma, 2007.