3Rs e i prodotti del futuro
Act Now for the Sustainable Development
Goals - SDGs in STEM Education
Maria Zambrotta
IIS Santorre di Santarosa - Torino
e-mail: maria.zambrotta@santorre.it
Indice
2. Introduzione all’unità didattica (n. 2): cosa si può fare con la lana?
3. Parte sperimentale sulla cheratina
Abstract. The work 3Rs and the product of the future, developed by the three authors Iro koliakou, Anders Floren and Maria Zambrotta, aims to stimulate reflection on more sustainable productions, starting with both raw and recycled materials. The abbreviation “3 R’s” stands for Reduce, Reuse, and Recycle and encapsulates the aims of the activities: the impact of daily plastic use is highlighted, several workshop activities on the study and reuse of wool, and the production of cement from mussel shells are presented. The goals are to engage students in active learning and stimulate their critical thinking.
In the online publication curated by Science on Stage, the following three sections are developed: (1) Bioplastics concerning an in-depth look at the use of plastics and the production of bioplastics; (2) Wool as a resource; in this regard some teaching units are published on wool as a raw material for bio-based products and the production of different products through simple chemistry experiments are reported; (3) How to make cement from mussel shells in which the production of cement using biomaterials is illustrated.
In this article will be presented only the section related to the Wool.
Keywords: lana; bioplastiche; biomassa; cheratina; Agenda 2030
L’unità presentata di seguito è parte integrante di un lavoro più ampio sviluppato da diversi autori, sotto il coordinamento di Science on Stage - Europe.
Le attività nascono con l’obiettivo di coinvolgere gli studenti in un apprendimento attivo, di coltivare il loro pensiero critico e di spingerli a riflettere su processi più sostenibili, per produrre oggetti di uso quotidiano, sia da materiali grezzi che da materiali riciclati.
L’abbreviazione “3R” sta per Ridurre, Riutilizzare e Riciclare e racchiude le finalità dei percorsi: viene messo in evidenza l’impatto dell’uso quotidiano della plastica, vengono presentate diverse attività di laboratorio sullo studio e il riuso della lana e sulla produzione di cemento da gusci di mitili.
Le attività partono da un questionario, per verificare le conoscenze degli studenti sui concetti di base dell’economia circolare, seguite, poi, da tre unità didattiche, elaborate da diversi autori, che possono essere anche svolte separatamente.
Una panoramica dell’intera attività, presentata direttamente dagli autori, è in un webinar disponibile al link https://youtu.be/8-JnIxsesWA, mentre il lavoro completo è reperibile al link: https://www.science-on-stage.eu/act-now-sdg.
Di seguito viene presentata l’unità didattica numero 2 che è stata elaborata dall’autrice del presente articolo.
2. Introduzione all’unità didattica (n. 2): cosa si può fare con la lana?
Le diverse esperienze proposte sono frutto di una collaborazione con l’ITS TAM (Tessile, Abbigliamento, Moda) di Biella e nascono da una riflessione sul mercato della lana e la gestione degli scarti. Le attività possono essere inserite in diversi percorsi curriculari:
Le attività di laboratorio e gli approfondimenti disciplinari possono essere proposte nella Scuola Secondaria sia di primo grado che di secondo grado.
2.1 Il mercato della lana
La lana di pecora è sempre stata utilizzata come prodotto agricolo dalle comunità pastorali, ma nel 2002, a seguito di una legge europea, la lana ha cambiato il suo status; il vello è passato da prodotto agricolo a materiale di categoria 3 (identificato come rifiuto). Da allora la lana sporca deve essere ripulita in centri specializzati per ridurre la presenza di batteri.
Le fasi del processo sono ben descritte dai Regolamenti europei, il Reg. 1069/2009 che abroga il Regolamento (CE) n. 1774/2002 e nel suo recepimento da parte degli Stati membri.
La tosatura delle greggi è un atto che gli allevatori devono compiere almeno una volta all’anno per mantenere il benessere dell’animale, ma poiché la lana ha diminuito il suo potere economico sul mercato europeo, è diventata per la maggior parte delle aziende agricole solo un costo.
Per rivalutare il prodotto e il mercato, negli ultimi anni sono state sempre più numerose le ricerche accademiche e industriali finalizzate allo sfruttamento della lana come biomassa e fonte di cheratina [[1], [2], [3]].
Un interessante approccio da proporre agli studenti potrebbe anche essere l’analisi del problema partendo da un punto di vista storico, come suggerito dagli autori del CNR di Biella [4], per arrivare alle nuove ricerche innovative [5].
2.2 Studio delle caratteristiche morfologiche e della composizione biochimica della lana
La lana è una fibra tessile naturale che si ricava principalmente dal vello di pecore, da alcuni tipi di capre e conigli. È composta principalmente da circa l’82% di proteine cheratiniche ad alto contenuto di cistina localizzate negli strati di squame e corteccia, dal 17,2% di proteine non cheratiniche a basso contenuto di cistina e da circa lo 0,8% di materiali non proteici sulla superficie dello strato di squame [6].
Dal punto di vista morfologico la fibra laniera è costituita da uno strato esterno composto da cellule piatte sovrapposte, una struttura interna e un midollo.
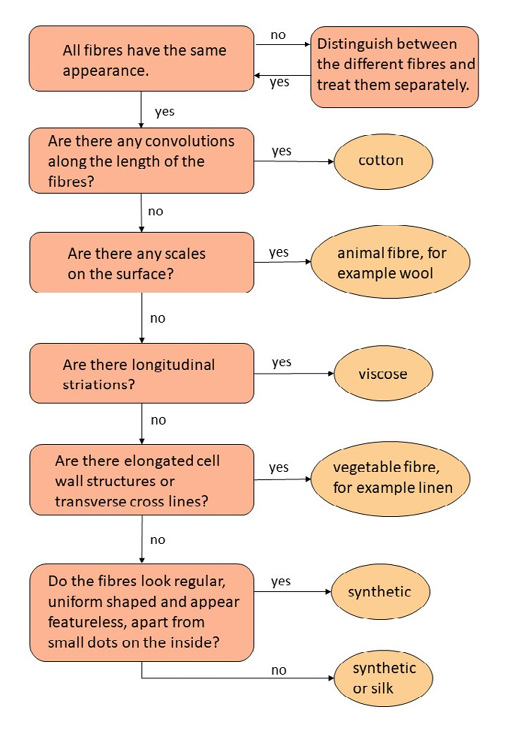
Un’interessante attività da proporre agli studenti è la distinzione tra le fibre naturali, come lana, cotone o lino, e le fibre artificiali mediante l’osservazione con un microscopio. Si possono, infatti, differenziare confrontando la vista longitudinale e la vista in sezione trasversale: in vista longitudinale, la lana appare cilindrica, irregolare, ha una superficie ruvida, una struttura squamosa e può apparire un midollo scuro sulle fibre di lana grossolana; nella vista in sezione trasversale, la lana si presenta quasi rotonda o circolare e può comparire un midollo [7].
Può essere di aiuto fornire agli studenti una guida all’osservazione simile a quella riportata in figura 1, reperibile sul sito https://www.science-on-stage.eu/material/3-rs-keratin.

Figura 1. Guida per l’osservazione al microscopio delle fibre (https://www.science-on-stage.eu/material/3-rs-keratin)
2.3 Composizione chimica della lana ed estrazione della cheratina
Il primo utilizzo della cheratina per scopi medici dovuto all’erborista cinese Li Shi Zhen risale al XVI secolo. La parola “cheratina” è apparsa per la prima volta in letteratura intorno al 1850 per descrivere il materiale di cui sono composti i tessuti duri. Nel 1905, John Hoffmeier negli Stati Uniti descrisse il processo di estrazione della cheratina dalle corna degli animali utilizzando la calce. Lo sviluppo delle tecniche nell’ultimo secolo in termini di processo di estrazione, purificazione e caratterizzazione delle proteine della cheratina ha portato alla preparazione di biomateriali a base di cheratina nell’industria farmaceutica, medica, cosmetica e biotecnologica [8].
L’attività sperimentale proposta consiste di una prima parte che riguarda propriamente la cheratina e di una seconda parte che, invece, si focalizza su alcuni metodi per tingere la lana.
3. Parte sperimentale sulla cheratina
3.1 Estrazione della cheratina (link al video: https://youtu.be/KIR3pSXrUPQ)
Materiali
Metodo
Pesare 5 g di lana grezza in un becher, ricoprirle con la soluzione di idrossido di sodio (150 ml) e mescolare la miscela con la bacchetta di vetro. Assicurarsi che la lana sia completamente coperta dalla soluzione di estrazione (Figura 2). Lasciare riposare per qualche ora. Se il tempo lo consente, attendere due ore prima dell’estrazione della cheratina. Se non è possibile aspettare, un periodo di 30 minuti permette già di avere un risultato sufficiente (Figura 3).
Il tempo indicato (idealmente 1 ora, o almeno 30 minuti) si riferisce all’ipotesi di una soluzione 1,0 M di NaOH; in alternativa, si può usare una soluzione meno concentrata (0,1 M) e lasciarla riposare per una notte. È meglio lavorare sotto cappa.

Figura 2. Lana prima dell’estrazione (https://www.science-on-stage.eu/material/3-rs-keratin)

Figura 3. Lana dopo l’estrazione (https://www.science-on-stage.eu/material/3-rs-keratin)
Analisi dei risultati
Trascorso il periodo di estrazione si propone agli studenti di estrarre dalla soluzione una parte delle fibre e osservarne l’aspetto.
Vengono proposte le seguenti domande guida.
Risposta possibile: colore bianco, morbida, con o senza arricciature.
Risposta possibile: la lana assume un colore scuro e un aspetto gelatinoso.
Risposta possibile: la soluzione chiara e incolore dell’inizio diventa scura e torbida.
Ulteriori domande di indagine da proporre agli studenti possono essere quelle riportate di seguito.
Risposta possibile: i cambiamenti osservati nell’aspetto delle fibre, sia in termini di cambiamento di colore che di torbidità della soluzione, indicano che si sono verificate reazioni chimiche.
Risposte possibili: la soluzione di NaOH ha un pH basico e, quindi, le catene di cheratina perdono la loro struttura 3D (denaturazione) e le fibre si dissolvono rendendo la soluzione gelatinosa; il colore scuro è causato dalla degradazione di alcuni aminoacidi; la cheratina può essere estratta senza degradarla, ma il processo di estrazione è piuttosto lungo e quindi difficile da realizzare in laboratorio; l’estrazione non degradativa viene effettuata utilizzando altri eluenti come, ad esempio, metabisolfito di sodio ed urea.
Per completare il lavoro sperimentale si potrebbero introdurre anche altri esperimenti di semplice realizzazione sulla denaturazione delle proteine.
3.2 Flocculazione della cheratina (link al video: https://youtu.be/KIR3pSXrUPQ)
Materiali
Metodo
Predisporre 4 provette uguali all’interno di un portaprovette. Versare all’interno della prima provetta 10 ml di acetone, nella seconda 10 ml di etanolo, nella terza 10 ml di succo di limone e, infine, nella quarta 10 ml di aceto o acido acetico 1 M. È necessario filtrare il succo di limone prima di usarlo per ridurre la torbidità. L’acido citrico in soluzione al 6% ha un valore di pH simile al succo di limone; perciò, volendo, si potrebbe usare al posto di quest’ultimo.
Segnare con il pennarello il nome della sostanza sulla provetta in cui è contenuta. In seguito, determinare il pH delle diverse soluzioni usando la cartina di tornasole (Figura 4).

Figura 4. pH delle diverse soluzioni (https://www.science-on-stage.eu/material/3-rs-keratin)
Aggiungere goccia a goccia in ciascuna provetta circa 2 ml della soluzione di estrazione (Figura 5).

Figura 5. Flocculazione con diversi solventi (https://www.science-on-stage.eu/material/3-rs-keratin)
Completare la tabella sottostante con le osservazioni (nella tabella sono riportate come esempio le osservazioni effettuate da alcuni studenti).
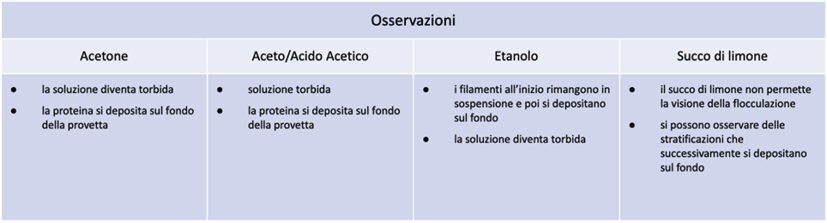
Possibili spunti di discussione:
Versare successivamente il contenuto di ciascuna provetta in una capsula di Petri e lasciare evaporare fino a completa essicazione, al fine di ottenere l’estratto di cheratina.
3.3 Precipitazione della cheratina
Dopo aver osservato gli effetti dei diversi tipi di solventi, si può procedere alla precipitazione della cheratina dall’intera soluzione di estrazione (Figura 6), aggiungendo sotto cappa pochi ml di acido acetico 1 M fino al raggiungimento del punto isoelettrico (pI= 4,2 - 4,5).

Figura 6. Precipitazione della cheratina (https://www.science-on-stage.eu/material/3-rs-keratin)
Successivamente si separa la cheratina mediante filtrazione con un colino, si trasferisce il filtrato su un vetrino da orologio e si lascia asciugare.
3.4 Preparazione di un balsamo per capelli con la cheratina
L’ultima attività proposta è stata la realizzazione di un balsamo partendo dalla cheratina estratta. Per una migliore riuscita in classe sarebbe meglio comprare la cheratina come soluzione al 25% m/V di cheratina in glicerina.
Materiali per ottenere 50 ml di prodotto
Metodo
Pesare tutti gli ingredienti in un becher, scaldare a bagnomaria fino alla fusione degli ingredienti. Aggiungere 1-2 gocce di olio essenziale e trasferire il prodotto ottenuto in un contenitore per l’utilizzo (Figura 7).

Figura 7. Balsamo ottenuto dalla cheratina (https://www.science-on-stage.eu/material/3-rs-keratin)
4. Parte sperimentale sulla tintura della lana
La tintura naturale dei tessuti risale a epoche antichissime, quando l’uomo primitivo cominciò a decorare con i colori i propri abiti e le coperte necessari a ripararsi dalle intemperie. Studi archeologici rivelano che gli uomini vennero a conoscenza dell’uso del colore nella pittura già nel 25.000 a.C., come testimoniato dai celebri disegni rinvenuti nelle grotte di Altamira (Spagna) e Lascaux (Francia). Ad oggi non conosciamo con precisione quando le tecniche pittoriche furono applicate alla tintura dei tessuti, ma reperti archeologici dell’epoca neolitica, come quelli rinvenuti nei villaggi di Ledro in Trentino, fanno presupporre con una certa approssimazione che gli uomini iniziarono a tingere il tessuto intorno al 3.000 a.C., in concomitanza con il passaggio dal nomadismo alla vita stanziale [9].
Un’ulteriore attività che viene presentata agli studenti è quella di tingere la lana con coloranti di origine naturale. Essa persegue due finalità: studiare le caratteristiche dei coloranti naturali e alcune tecniche di tintura delle fibre tessili e rendere la lana di scarto esteticamente più gradevole.
I coloranti naturali sono generalmente costituiti da molecole organiche dotate di cromofori in grado di assorbire le lunghezze d’onda della luce nella zona del visibile, oppure di manifestare questa proprietà quando si legano al tessuto e/o ad altre sostanze, come ad esempio particolari ioni metallici. Vengono estratti da piante, invertebrati marini, alghe, nonché prodotti da batteri e funghi. Si possono acquistare in estratto o in polvere e da ogni pianta si possono ottenere un numero considerevole di sfumature diverse [10], [11].
Generalmente, i coloranti vengono classificati in base a due criteri: alla composizione chimica o alla modalità di impiego. Una classificazione dei coloranti secondo la tipologia del processo impiegato per la loro applicazione prevede la distinzione nelle due seguenti categorie [12].
4.1 Tintura diretta con curcuma (link al video: https://youtu.be/7Mkj_MPMogE)
La curcuma si ottiene dai rizomi seccati e polverizzati della Curcuma domestica Valeton (Curcuma longa), o da varie altre specie di Curcuma come la Curcuma tinctoria e la Curcuma viridiflora Roxb. Nei rizomi della curcuma sono presenti tre composti principali responsabili del colore: curcumina, demetossicurcumina e bis-demetossicurcumina [12], noti collettivamente come curcuminoidi, riportati in figura 8. La curcumina è un colorante diretto, ma può anche essere utilizzato come colorante a mordente grazie alle caratteristiche di-chetoniche del composto.
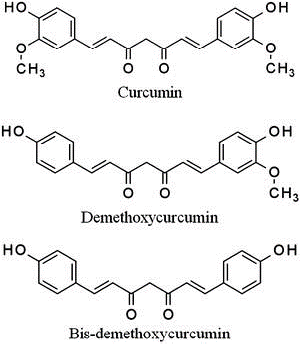
Figura 8. Formula chimica dei composti presenti nella curcuma (fonte [12])
Materiale
Metodo
Per preparare la tintura, è necessario utilizzare la radice di curcuma tritata, o la polvere, in una quantità pari al 50% del peso del filato secco. Pesare 25 g di polvere di curcuma e trasferirli in un becher da 500 ml. Aggiungere 250 ml di acqua e mescolare accuratamente con una bacchetta di vetro. Trasferire il becher in un bagnomaria e lasciare scaldare per 30 minuti a fuoco moderato. Raffreddare il bagno di tintura, attendere qualche minuto che il solido decanti per quanto possibile sul fondo del recipiente e trasferire il surnatante su filtro a pieghe usando un becher pulito per raccogliere il filtrato. Riempire un contenitore capiente, ad esempio un cristallizzatore, con acqua fredda sufficiente a coprire la fibra (2 litri ogni 50 g di lana), unire la soluzione di curcuma e mescolare; immergere quindi la lana nel bagno di tintura e scaldare per 30 minuti a fuoco moderato. Far raffreddare, prelevare la lana dal bagno al raggiungimento dell’intensità di colore desiderata, risciacquare sotto acqua corrente, strizzare e tamponare con carta assorbente (Figura 9) [13].

Figura 9. Lana tal quale e lana colorata con curcuma (https://www.science-on-stage.eu/material/3-rs-keratin)
4.2 Tintura a mordente con cavolo rosso (link al video: https://youtu.be/5miWV3BhcNU)
Nel caso della tintura della lana con cavolo rosso deve essere prima effettuata la mordenzatura per garantire l’ottimale fissaggio delle sostanze idrosolubili presenti nel bagno di tintura. Sono di seguito riportati le operazioni condotte per le diverse fasi della tintura.
Fase 1: mordenzatura della lana
Materiale
Metodo
Immergere in acqua la lana precedentemente lavata, tre minuti prima di iniziare il processo di tintura.
Mettere a scaldare circa 200 ml di acqua in un becher. Aggiungere ai 200 ml di acqua 15 g di allume e 5 di cremor tartaro e mescolare per solubilizzare.
Versare in un cristallizzatore 2 litri di acqua ogni 100 g di lana asciutta, aggiungere la soluzione mordenzante e immergere la lana messa a bagno.
Far bollire per 1 ora e mescolare frequentemente, quindi, lasciare raffreddare la lana, lentamente e naturalmente, lasciandola nella soluzione mordenzante.
Risciacquare molto bene la lana con acqua fredda o tiepida.
Se non è possibile tingere subito la lana, conservare i campioni mordenzati in frigorifero avvolti in una carta. Ricordare che i contenitori utilizzati devono essere in acciaio inossidabile o vetro. L’alluminio è sconsigliato perché può alterare i colori [14],[15].
Fase 2: preparazione del decotto di cavolo rosso
Il cavolo rosso deve il suo colore alla presenza nelle sue foglie di antocianine, che impartiscono il colore anche a molti frutti e molti fiori. Sebbene siano note centinaia di molecole differenti appartenenti alla classe delle antocianine, esse sono tutte costituite dallo stesso nucleo centrale (Figura 10). Ad esso possono essere legati residui di zuccheri e, talvolta, di acidi carbossilici. Anche qualcuno degli atomi di idrogeno legati agli atomi di carbonio può essere sostituito da altri gruppi di atomi diversi. Per un approfondimento della chimica organica di questa classe di composti si rimanda ai lavori citati in bibliografia [16], [17],[18].
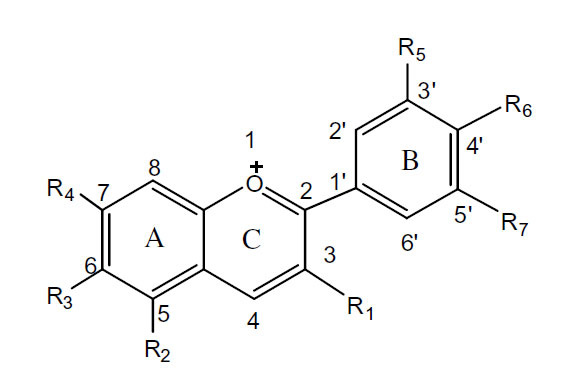
Figura 10. Struttura chimica del nucleo centrale di una antocianina (fonte [16])
Materiale
Metodo
Tagliare il cavolo a strisce sottili e metterlo in un contenitore con acqua a 60 °C, riscaldando ulteriormente per circa ٣٠-٤٠ minuti per estrarre gli antociani, evitando di raggiungere l’ebollizione per impedire la decomposizione delle antocianine, instabili alle alte temperature [18].
Il peso del cavolo deve essere 60 volte quello del tessuto da tingere.
Filtrare il liquido di estrazione del cavolo rosso per le operazioni di tintura.
Fase 3: Tintura della lana
Versare il liquido ottenuto dalla precedente estrazione in un contenitore capiente, ad esempio un cristallizzatore, scaldare a una temperatura di 40 °C e immergervi completamente la lana mordenzata, per assicurarsi che tutte le fibre assorbano l’acqua di tintura.
Impostare il fuoco medio-basso e lasciare la lana in ammollo nella pentola per almeno un’ora o anche più a lungo per ottenere un colore più intenso. È molto importante non far bollire il liquido durante questa fase.
Quindi togliere la lana dal bagno di colore, risciacquarla delicatamente, stenderla e lasciarla asciugare per una notte.
Il colore ottenuto dal cavolo rosso varia a seconda del pH e del tessuto: a pH acido si ottiene un colore rossastro, mentre a pH basico un colore verdognolo. Ulteriori spiegazioni del processo sono riportate in un lavoro divulgativo dell’ENEA [19].
Il percorso proposto ha permesso di applicare le conoscenze curriculari di chimica organica al mondo reale e industriale. Inoltre, l’approccio laboratoriale e cooperativo ha portato dei risultati positivi soprattutto per l’aumento di interesse nei ragazzi meno motivati.
[1] https://elearning.fondazioneuniversitaria.it/pluginfile.php/2562/mod_resource/content/0/Il%20riutilizzo%20degli%20scarti%20di%20lana%20%20-%20Fac.%20Med%20Veterinaria.pdf
[2] http://lifewolfalps.eu/wp-content/uploads/2021/02/C7_Relazione-tecnica_lana_2020_12.pdf
[3] C. Tonin, Ricerca-e-innovazione-per-nuovi-ri-utilizzi-della-lana-il-progetto-life-greenwoolf.html
[4] https://rmschools.isof.cnr.it/wp-content/uploads/2021/12/IT_4_Renewable-Keratin-Wastes-in-Metal-Mining-APPENDIX-1.pdf
[5] https://www.researchgate.net/publication/221907431_Keratin-based_Nanofibres
[6] D. M. Lewis, J. A. Rippon (Eds.), The Coloration of Wool and other Keratin Fibres, Wiley&Sons, 2013; (https://scholar.google.com/scholar_lookup?title=The%20Coloration%20of%20Wool%20and%20other%20Keratin%20Fibres&publication_year=2013&author=D.M.%20Lewis&author=J.A.%20Rippon)
[7] https://www.textileschool.com/330/microscopic-appearance-of-fibres/
[8] M. Koleva, D. Zheleva, Journal of Chemical Technology and Metallurgy, 2022, 57(1), 76-83; (https://journal.uctm.edu/node/j2022-1/9_21-08p76-83.pdf)
[9] https://core.ac.uk/download/pdf/14703675.pdf
[10] https://www.mcurie.edu.it/files/leone.francesco/coloranti.pdf
[11] https://stmateriali.campusnet.unito.it/att/Presentazione_Davit_Gulmini_170217_1.pdf
[12] https://stmateriali.campusnet.unito.it/att/Dispense_laboratorio_def.pdf
[13] https://ricerca-scuola.ism.cnr.it/pluginfile.php/148/mod_resource/content/1/Lezione%202%20-%20pH%20sensing%20con%20curcuma.pdf
[14] https://thefeltstore.com/blogs/news/naturally-dyeing-wool-with-red-cabbage
[15] https://www.iisvaldagno.it/wp/wp-content/uploads/2014/06/Tinture-con-coloranti-naturali-AS-2013-2014.pdf
[16] B. Alappat, J. Alappat, Molecules, 2020, 25(23), 5500; (https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7727665/#B15-molecules-25-05500)
[17] B. Arik, E. Canitez, A. Kirtak, Journal of Natural and Applied Sciences, 2020, 24(2), 244-255; (https://dergipark.org.tr/en/download/article-file/843244)
[18] https://www.jstage.jst.go.jp/article/fsti9596t9798/2/1/2_1_30/_pdf/-char/en
[19] https://agenda.enea.it/event/183/contributions/1744/attachments/64/155/Dispense_per_insegnanti_Magia_della_Chimica.pdf